Que a manteiga é um produto lácteo maravilhoso nós já sabemos, mas de onde ela vem? Para começarmos a entender o que é essa riqueza, vamos do início.
Como ocorre a produção da manteiga?
A manteiga é fabricada há milhares de anos, a partir do creme de leite — ou a famosa nata —, que a partir de um processo para conservação do creme de leite, transformou-se em um dos ingredientes mais utilizados na culinária mundial, além de ser um produto consumido diretamente em pães, biscoitos e outras delícias (Deosarkar et al., 2016).
Encontramos no comércio diferentes tipos de manteiga: manteiga com e sem sal, manteiga maturada ou não maturada, manteiga extra, manteiga de primeira qualidade, manteiga comum e a tradicional manteiga de garrafa.
Atualmente, com o avanço das tecnologias e novas demandas do mercado consumidor, as indústrias têm investido em uma diversidade ainda mais ampla de opções, produzindo manteigas zero lactose, manteiga ghee e manteiga com flor de sal, que têm apresentado grande aceitabilidade, especialmente pelas características sensoriais específicas e apelo gastronômico.
Segundo a definição oficial, a manteiga é um produto gorduroso, obtido, exclusivamente, pela bateção do creme pasteurizado obtido de leite de vaca, composta por gordura láctea, água e proteínas do leite (Brasil, 1996).
Assim, o creme de leite pasteurizado é ingrediente obrigatório e fundamental para a fabricação de manteiga. O processo de produção ocorre comumente através do método de agitação por batelada, ilustrado na Figura 1.
Figura 1. Estágios de produção de manteiga. 1) bateção do creme resfriado; 2) bateção e separação do leitelho; 3) drenagem do leitelho e 4) malaxagem.
Fonte: os autores.
Para iniciar a produção da manteiga, o creme de leite pasteurizado deve estar resfriado entre 10 e 14 °C, para proporcionar a cristalização de parte da gordura. Em seguida, durante a agitação, ocorre a incorporação de ar e assim, inicia-se o desenvolvimento de grandes bolhas que formam uma espuma tipo chantilly.
Ao continuar o processo de agitação, essa espuma fica mais densa, e o tamanho das bolhas diminuem, envolvendo a gordura em uma interface ar/água. Devido à pressão que as bolhas de ar exercem sobre os glóbulos de gordura, suas membranas se rompem levando ao extravasamento de parte da gordura líquida, que permite a coalescência parcial dos glóbulos de gordura.
À medida que a agitação continua, glóbulos ainda íntegros começam a se aglomerar, formando uma rede com gordura cristalizada, gordura líquida e ar. A gordura líquida extravasada do glóbulo para o meio, age como aderente, que permite a formação de “grãos”. Estes grãos vão aumentando de tamanho devido ao seu encontro durante a turbulência do processo. No decorrer da agitação, os pequenos grãos de manteiga se tornam visíveis e, inicia-se a separação do leitelho.
Neste momento, ocorre a inversão de fases: a emulsão de óleo em água, que anteriormente caracterizava o creme, se transforma em uma emulsão de água em óleo, que caracteriza a manteiga (Walstra et al., 2005, Fox et al., 2015).
Em seguida, o leitelho é drenado, e iniciam-se as lavagens com água potável fria, para retirar o máximo possível de leitelho. Dependendo do mercado alvo, a manteiga pode passar por mais etapas de lavagem, e todo líquido descartado desse processo é considerado leitelho.
Após esta etapa, é feita a malaxagem (working), onde os grãos de manteiga são transformados em uma massa homogênea, e a incorporação final de água à massa e contribui para o controle do teor de umidade. Nesta etapa, podem ser adicionados ainda sal e corante, dependendo da característica do produto final. Posteriormente, a manteiga é destinada para embalagem.
O que é o leitelho?
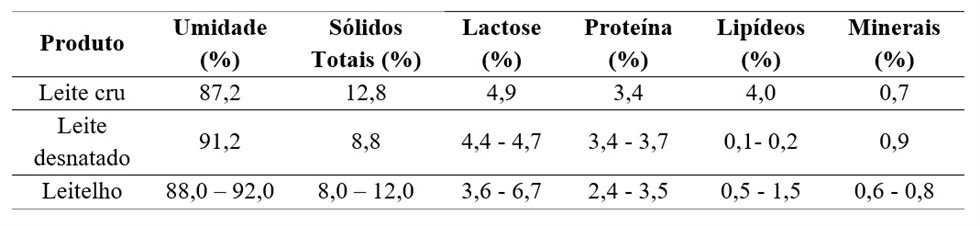
O leitelho, ou “soro da manteiga”, é o líquido esbranquiçado obtido durante a produção da manteiga, durante a etapa de bateção e inversão de fase, ilustrado na Figura 1. Como a matéria-prima para a fabricação da manteiga é o creme de leite, o leitelho contém resíduos de triglicerídeos e todos os componentes hidrossolúveis do creme de leite, como lactose, minerais como Ca, Mg e P, e o material presente na membrana do glóbulo de gordura (Corredig et al., 2003). A composição do leitelho é semelhante à do leite desnatado, com cerca de 90% de água e 1% de gordura (Tabela 1).
Tabela 1. Composição média (%) do leite cru, leite desnatado e leitelho.
Fonte: adaptado de Mistry et al. (1996), Sodini et al. (2006), Vanderghem et al. (2010).
Os lipídeos do leite são compostos por cerca de 98% de triglicerídeos, sintetizados no citoplasma da célula secretora dos alvéolos mamários, formando pequenos glóbulos que aumentam de tamanho e agregam componentes como proteínas e substâncias presentes no citoplasma da célula, ao serem transportados para a extremidade da célula secretora (Walstra et al., 2005).
No processo de excreção, os glóbulos de gordura são envolvidos por parte da membrana celular, formando o que chamamos de membrana do glóbulo de gordura do leite (MGGL), composta por cerca de 60% de proteínas e 40% de lipídeos (Fox et al., 2015).
Essa MGGL é o que torna o leitelho tão especial. Ela apresenta uma diversidade de proteínas e frações lipídicas com características nutricionais bastante interessantes, que contribuem na redução da absorção intestinal de colesterol, protege contra infecções causadas por bactérias e vírus, e dificulta ainda a aderência de patógenos à mucosa intestinal (Pfeuffer, 2001).
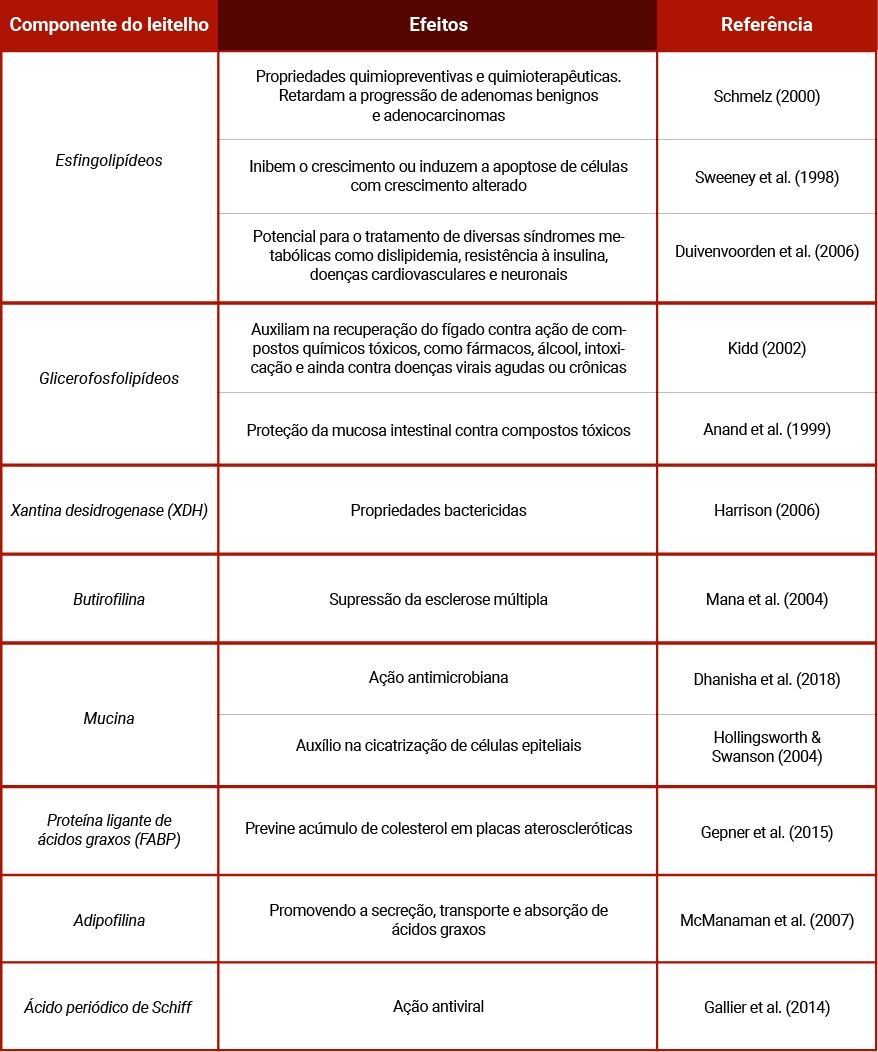
Os constituintes do leitelho estão associados ainda a redução de doenças cardiovasculares e neuronais, auxiliam o organismo na proteção contra microrganismos através do estímulo à resposta imune inata e na produção de muco, além de outros efeitos, apresentados na Tabela 2.
Tabela 2. Principais componentes do leitelho e seus efeitos benéficos à saúde.
Por que não devemos jogar o leitelho fora?
O que tem acontecido nos últimos anos é uma mudança na percepção sobre a ingestão da gordura do leite, que por muitos anos foi considerada vilã na alimentação humana e que agora tem sido considerada aliada.
Isso tem levado a um aumento no consumo de creme de leite e, principalmente, manteiga, contribuindo para o aumento da sua demanda de mercado. Esse crescimento, consequentemente, gera aumento na produção de leitelho.
O leitelho apresenta uma alta Demanda Bioquímica de Oxigênio (DBO), devido à alta concentração de matéria orgânica, sendo considerado altamente poluente e com potencial poluidor superior ao soro lácteo. Com isso, seu descarte incorreto pode alterar, significativamente, o meio ambiente, prejudicando sistemas de produção sustentáveis, que apontam para a conservação de recursos naturais.
A utilização do leitelho como matéria-prima ou ingrediente na fabricação de outros alimentos pode ser benéfica em relação aos aspectos tecnológicos, nutritivos e funcionais do produto. Comumente, o maior uso do leitelho em alimentos está relacionado à tecnologia de produção, por ser considerado um eficiente emulsificante natural. Isto ocorre, em especial, pela presença dos fosfolipídios na MGGL, que apresentam uma parte hidrofílica, que interage com a fase aquosa, e uma parte lipofílica, que permite a interação com a fase oleosa.
Desta forma, o uso do leitelho tem sido explorado para substituir o uso de emulsificantes comerciais como a lecitina (Jukkola et al., 2019). A sua maior aplicabilidade tem sido relacionada a derivados lácteos como iogurtes e queijos, melhorando a textura, rendimento, características sensoriais e vida de prateleira (Saffon et al., 2013; Hickey et al., 2017; Skryplonek et al., 2019).
No Brasil, várias indústrias já compreenderam os benefícios nutricionais, tecnológicos e ambientais do uso do leitelho e têm adicionado, de maneira gradual, este co-produto tão valioso da indústria láctea em derivados lácteos e outros alimentos. Mas, infelizmente, muitas indústrias de laticínios ainda jogam essa riqueza ralo abaixo.
Agora que você conhece melhor o leitelho, seus benefícios e potenciais, que tal repensar o seu uso na indústria?
Agradecimentos
Os autores agradecem ao Centro de Pesquisa em Alimentos da Escola de Veterinária e Zootecnia da UFG pelo apoio ao ensino, extensão, pesquisa e sua divulgação.
Referências
Anand BS., Romero JJ., Sanduja SK. LL. Phospholipid association reduces the gastric mucosal toxicity of aspirin in human subjects. Am J Gastroenterol. 1999; 94:1818–22.
Brasil, Ministério da Agricultura, Pecuária e Abastecimento. Portaria nº 146 de 7 de março de 1996. Publicado no Diário Oficial da União em 11/03/1996, nº 48, seção 01.
Corredig M, Roesch RR, Dalgleish DG. Production of a Novel Ingredient from Buttermilk. J Dairy Sci. 2003; 86(9):2744–50.
Deosarkar SS, Khedkar CD, Kalyankar SD. Butter: Manufacture. Encycl Food Heal. 2016; 529–34.
Dhanisha S, Guruvayoorappan C, Drishya S, Abeesh P. Mucins: Structural diversity, biosynthesis, its role in pathogenesis and as possible therapeutic targets. Crit Rev Oncol Hematol. 2018; 122:98–122.
Duivenvoorden I., Voshol PJ., Rensen PCN., Van Duyvenvoorde W. RJ, JJ. E. Dietary sphingolipids lower plasma cholesterol and triacylglycerol and prevent liver steatosis in APOE*3Leiden mice. Am J Clin Nutr. 2006; 84:312–21.
Fox PF, Uniacke-Lowe T, McSweeney PLH, O’Mahony JA. Dairy chemistry and biochemistry. 2015. 584 p.
Gallier S, Laubscher A, Jiménez-Flores R. The Milk Fat Globule Membrane: Structure, Methodology for its Study, and Functionality. Food Struct Dig Heal. 2014; 107–42.
Gepner A, Young R, Delaney J, Tattersall M, Blaha M, Post W, et al. Comparison of coronary artery calcium presence, carotid plaque presence, and carotid intima-media thickness for cardiovascular disease prediction in the multi-ethnic study of atherosclerosis. Circ Cardiovasc. 2015; 8(1):e002262.
Harrison R. Milk xanthine oxidase: properties and physiological roles. Int Dairy Sci. 2006; 16:546–554.
Hickey CD, Diehl BWK, Nuzzo M, Millqvist-Feurby A, Wilkinson MG, Sheehan JJ. Influence of buttermilk powder or buttermilk addition on phospholipid content, chemical and bio-chemical composition and bacterial viability in Cheddar style-cheese. Food Res Int. 2017; 102:748–58.
Hollingsworth M, Swanson B. Mucins in cancer: protection and control of the cell surface. Nat Rev Cancer. 2004; 4:45–60.
Jukkola A, Partanen R, Xiang W, Heino A, Rojas O. Food emulsifiers based on milk fat globule membranes and their interactions with calcium and casein phosphoproteins. Food Hydrocoll. 2019; 94:30–7.
Kidd P. Phospholipids: Versatile nutraceutical ingredients for functional foods. Funct Foods Nutraceuticals. 2002; 12:30–40.
Mana, P., M. Goodyear, C. Bernard, R. Tomioka, M. Freire-Garabal, and D. Linares. Tolerance induction by molecular mimicry: Prevention and suppression of experimental autoimmune encephalomyelitis with the milk protein butyrophilin. Int. Immunol. 2004; 16:489–499.
McManaman J, Zabaronick W, Schaack J, Orlicky D. Lipid droplet targeting domains of adipophilin. J Lipid Res. 2003; 44 (4):668–73.
Mistry V, Metzger L, Maubois J. Use of ultrafiltered sweet buttermilk in the manufacture of reduced fat cheddar cheese. J Dairy Sci. 1996; 79:1137–45.
Pfeuffer M SJ. Dietary sphingolipids: Metabolism and potential health implications. Kieler Milchwirtsch Forschungsberichte. 2001;53(1):31–40.
Saffon M, Richard V, Jim enez-flores R, Gauthier S F BM and, Y P. Behavior of heat-denatured whey: buttermilk protein aggregates during the yogurt-making process and their influence on set-type yogurt properties. Foods. 2013; 2:444–459.
Schmelz E. M. Dietary sphingomyelin and other sphingolipids in health and disease. Nutr Bull. 2000; 25:135–139.
Skryplonek, K., Dmytrów, I., & Mituniewicz-Malek A. The use of buttermilk as a raw material for cheese production. Int J Dairy Technol. 2019; 72(4):610-616
Sodini I, Morin P, Olabi A, Jiménez-Flores R. Compositional and functional properties of buttermilk: a comparison between sweet, sour, and whey buttermilk. J Dairy Sci. 2006; 89:525–36.
Sweeney EA, Inokuchi J IY. Inhibition of sphingolipid induced apoptosis by caspase inhibitors indicates that sphingosine acts in an earlier part of the apoptotic pathway than ceramide. FEBS Lett. 1998; 425:61–5.
Vanderghem C, Bodson P, Danthine S, Paquot M, Deroanne C, Blecker C. Milk fat globule membrane and buttermilks: from composition to valorization. Biotechnol Agron Soc Environ. 2010;14(3):485–500.
Walstra P, Wouters, JTM, Geurts TJ. Dairy science and technology. 2005, 808p.