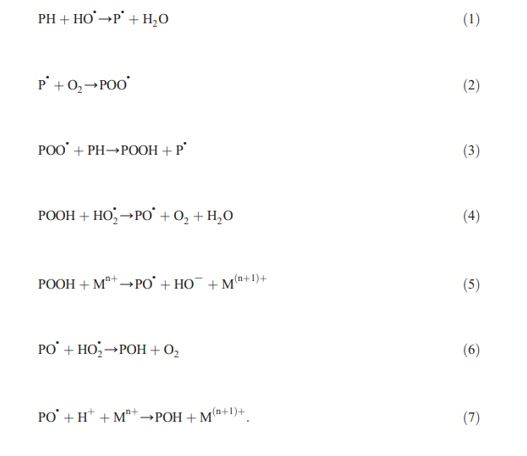O leite é um alimento muito presente na vida do brasileiro, e que, assim como outros alimentos, pode sofrer alterações físicas e químicas responsáveis pela diminuição de seu tempo de vida útil e mudanças em características sensoriais como o sabor.
O potencial de alteração da composição e das propriedades físico-químicas do leite é tido como uma das ferramentas estratégicas que podem ser utilizadas pelos produtores para aumentar a eficiência em destinar produtos que se adéquem às diferentes necessidades do consumidor (Cruz et al., 2017) e induz a indústria de laticínios a produzir alimentos de alta qualidade para se adequar à procura do mercado.
A busca por um produto de qualidade está diretamente relacionada ao conhecimento acerca dos componentes do leite e a forma como eles se equilibram, permitindo a compreensão das alterações ocorridas desde o manejo produtivo até as etapas tecnológicas dentro da indústria.
Nos últimos anos, muitos estudos foram realizados com o objetivo de elucidar se estas alterações ocasionadas por defeitos tecnológicos estariam ligadas a processos oxidativos. Ainda, responder se o desenvolvimento de oxidação poderia ser um fator limitante à estipulação do tempo de prateleira dos produtos lácteos e quais as consequências da oxidação nestes produtos.
O princípio básico do processamento UHT é a preservação dos alimentos líquidos pela exposição dos mesmos a um calor intenso por um rápido período, destruindo assim os microrganismos que possam estar contidos no produto (Zabbia et al., 2012).
Um tipo de defeito tecnológico comumente relatado é a alteração de características sensoriais, ou seja, modificações de sabor. As principais alterações neste aspecto são os sabores: Stale ou envelhecido; cooked ou maltado; lipolítico ou rançoso e amargo (Zabbia et al., 2012).
O fenômeno oxidativo é um conjunto de reações químicas responsáveis por diversos tipos de deterioração de alimentos e que resultam em mudanças desfavoráveis no sabor e odor, além de diminuição de segurança, valor nutritivo dos alimentos e vida útil.
A velocidade e facilidade em que as reações de oxidação acontecem dependem de inúmeros fatores, tais como: quantidade e tipo de ácido graxo constituinte, e tipo de proteína; concentração de oxigênio presente, umidade do produto, presença de pró-oxidantes e antioxidantes (Aldini et al., 2015).
O processo de oxidação se inicia quando um radical livre extremamente reativo (em busca de estabilidade) retira um átomo de hidrogênio do grupo metileno da cadeia do ácido graxo, gerando assim um radical alquil (L*).
Em seguida ocorre a fase de propagação que se dá em forma de reação em cadeia. O radical alquil é instável e se liga ao oxigênio, formando assim um radical peroxila (LOO*). Este, também buscando estabilidade energética, fará a remoção de hidrogênio de outro ácido graxo, gerando assim mais radicais livres. Assim, subsequentemente serão formados os produtos primários da oxidação lipídica (Figura 1) – os hidroperóxidos (LOOH) (Johnson et al., 2015).
Figura 1. Esquema da evolução da oxidação lipídica (Johnson et al., 2015).
Por muito tempo os estudos sobre a oxidação lipídica dos alimentos foram priorizadas por ser considerada a principal causa de deterioração microbiológica. Atualmente, em consequência a estudos de outras áreas, como a medicina e o esporte, pesquisadores de alimentos de origem animal têm redirecionado os estudos em oxidação para as proteínas e os impactos na alimentação humana. Por serem pesquisas relativamente novas, ainda são escassos os estudos conclusivos e específicos sobre oxidação proteica do leite.
A oxidação proteica se inicia quando um radical peroxil (LOO*), proveniente de oxidação lipídica se associa a proteínas, formando um radical proteico (P*). Este radical em presença de oxigênio formará rapidamente um radical peroxil proteico (POO*), que por sua vez, também buscando estabilidade, procurará outro alvo proteico formando compostos primários de oxidação como hidroperóxidos proteicos (POOH*), radicais alcoxil (PO*) e derivados proteicos hidroxil (POH*) (Figura 2). Estes radicais em associação com metais de transição como Mn+, Cu+ e Fe2+ se dissipam e formam os compostos secundários como as carbonilas (aldeídos e cetonas) (Estévez, 2011).
Figura 2. Sequência de reações de formação de radicais livres (Estévez, 2011).
As proteínas no leite podem sofrer carbonilação (introdução de monóxido de carbono) de três diferentes modos. No primeiro, compostos dicarbonílicos como glioxal (GO), metil-glioxal (MGO) e 3-deoxiglucosona (3-DG), são formados quando ocorre reações de Maillard ou por oxidação de açúcares, ou de lipídios (Santos et al., Botelho, Oliveira de., 2008).
Estas moléculas são extremamente reativas e podem provocar modificações em cadeias laterais de lisina, arginina e em resíduos de cisteína. Na segunda forma, os mesmos resíduos interagem com os resíduos de oxidação lipídica como acroleína, malondialdeído, 2-heptanona e 4-hidroxil-2-nonenal (HNE).
Estas duas últimas moléculas são apontadas por fazer parte do grupo conhecido como metil cetonas (aldeídos alifáticos) e são associadas ao aroma “envelhecido” do leite UHT. Na terceira forma, íons metálicos, como o cobre, podem acelerar a oxidação de aminoácidos como lisina, arginina, prolina e treonina (Milkovska et al., 2017).
Além da carbonilação, a oxidação de grupos tiol (biomarcadores de estresse oxidativo) como cisteína e metionina, levam a perda de grupos sulfidrilas, gerando compostos sulfidrílicos como ácido sulfínico (RSOOH) e dissulfetos (RSSR) formados a partir de ligações cruzadas (Milkovska et al., 2017).
No leite UHT estes grupos sulfidrílicos também são formados como consequência da desnaturação térmica de moléculas de β- lactoblobulina após processamento. Compostos gerados como sulfeto de hidrogênio são apontados como responsáveis pelo sabor “cozido” do leite UHT (Milkovska et al., 2017).
Em leite sabe-se que lipídios e proteínas possuem uma relação de equilíbrio peculiar, de forma que os tratamentos térmicos podem abalar essa relação de equilíbrio facilmente. Sendo assim, as proteínas são os componentes que sofrem as maiores alterações.
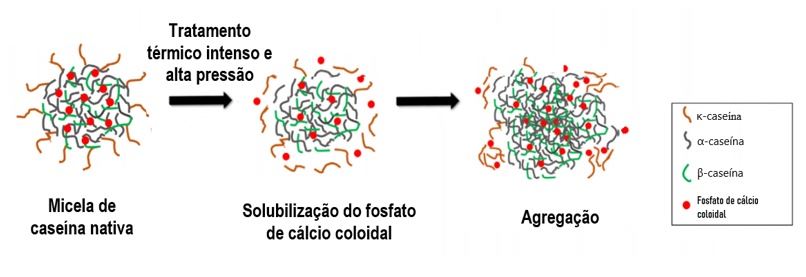
O processamento UHT desencadeia alterações na estrutura micelar da caseína, aumento no número de pequenas partículas micelares e na quantidade de caseínas solúveis (solubilização do fosfato de cálcio coloidal) o que contribui para uma agregação das partículas micelares (Figura 3) (Nunes et al., 2019). Essas micelas de caseína são as maiores responsáveis pela estabilidade térmica do leite.
Figura 3. Efeito dos tratamentos térmicos nas estruturas da micela de caseína.
Fonte: NUNES et al (2019).
Outra consequência é a desnaturação das proteínas do soro, principalmente a B-lactoglobulina. Estas proteínas desnaturadas juntamente com as modificações da K caseína formam um complexo que compromete a estabilidade da estrutura micelar, por interferir nas interações do fosfato de cálcio com as micelas.
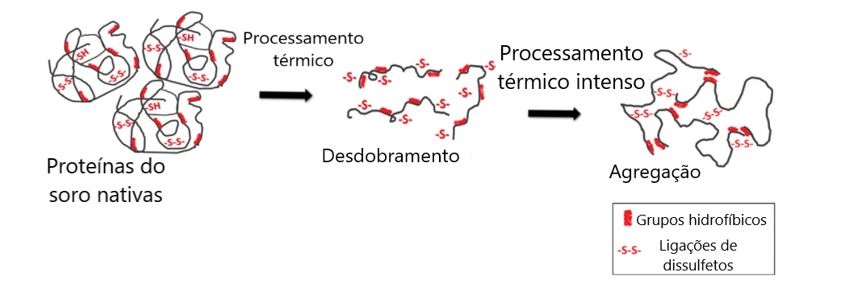
Essa instabilidade da estrutura micelar pode resultar em um material gelatinoso no leite (coágulo) e pode comprometer a digestão do leite no estômago e intestino (Borad et al., 2017). Para haver estabilidade deste complexo há a necessidade de compensação por interações hidrofóbicas, interações iônicas e ligações entre pontes de dissulfetos (Figura 4). (Milkovska et al., 2017).
Figura 4. Efeitos do tratamento térmico nas proteínas do soro.
Fonte: NUNES et al (2019).7
Desta forma pode haver modificações no balanço iônico suficiente para causar desestabilização das ligações carbono-hidrogênio nos ácidos graxos (principalmente os poli-insaturados). Assim resultar em toda a cascata oxidativa anteriormente mencionada.
O principal resultado do processamento térmico apontado pela literatura é a reação de Maillard. Esta reação gera compostos detentores de nitrogênio e enxofre como furanos, cetonas e pirazinas. Consequentemente, podem tanto influenciar diretamente a alteração de caracteres organolépticos (cor, sabor, consistência) quanto desencadear a reação oxidativa em cascata mencionada anteriormente (Milkovska et al., 2017).
A oxidação lipídica no leite não ocorre do mesmo modo que em outros produtos alimentícios. A composição complexa dos produtos lácteos, o estado físico do produto (líquido, sólido, emulsão, entre outros) e a presença de agentes anti e pró-oxidantes, bem como as condições de processamento e estocagem tendem a influenciar a taxa de auto oxidação (Vidal et al., 2018). Vários fatores podem influenciar no desenvolvimento de oxidação no leite. Na próxima coluna, falaremos sobre este assunto.
Autores:
Antônio dos Santos Neto, Médico Veterinário e Fiscal Estadual Agropecuário – Agência Goiana de Defesa Agropecuária - AGRODEFESA
Prof. Dr. Moacir Evandro Lage, Professor e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Ana Carolina Martinez de Oliveira, Graduanda em Medicina Veterinária e Participante do Programa de Iniciação Científica Voluntária LIP/CPA/ EVZ/UFG
Wanessa Ribeiro Gualdevi, Graduanda em Medicina Veterinária e Participante do Programa de Iniciação Científica Voluntária LIP/CPA/ EVZ/UFG
Eduarda Pereira Santana, Graduanda em Medicina Veterinária – EVZ/UFG
Profa. Dra. Clarice Gebara Muraro Serrate Cordeiro, Professora e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Profa. Dra. Francine Oliveira Souza Duarte, Professora e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Profa. Dra. Iolanda Aparecida Nunes, Professora e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Prof. Dr. Cristiano Sales Prado, Professor e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Profa. Dra. Cíntia Minafra, Professora e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/ EVZ/UFG
Profa. Dra. Valéria Quintana Cavicchioli, Professora e Pesquisadora do Laboratório de Inovação e Pesquisa LIP/CPA/EVZ/UFG
Referências
ALDINI G, Domingues MR, Spickett CM, Domingues P, Altomare A, Sánchez-Gómez FJ, et al. Protein lipoxidation: Detection strategies and challenges. Redox Biol. 2015;05(01):253–66.
BORAD SG, Kumar A, Singh AK. Effect of processing on nutritive values of milk protein. Crit Rev Food Sci Nutr. 2017;57(17):3690–702.
CRUZ A et al. Processamento de Leites de Consumo: Coleção Lácteos. Elsevier Brasil, 2017. In.
ESTÉVEZ M. Protein carbonyls in meat systems: A review. Meat Sci. 2011;89(03):259–79.
JOHNSON DR, Decker EA. The role of oxygen in lipid oxidation reactions: A review. Annu Rev Food Sci Technol. 2015;06(06):171–90.
MILKOVSKA-Stamenova S, Mnatsakanyan R, Hoffmann R. Protein carbonylation sites in bovine raw milk and processed milk products. Food Chem. 2017;229(01):417–24.
NUNES L, Tavares GM. Thermal treatments and emerging technologies: Impacts on the structure and techno-functional properties of milk proteins. Trends Food Sci Technol. 2019;90(01):88–9.
SANTOS-Zago LF, Botelho AP, Oliveira AC de. Os efeitos do ácido linoléico conjugado no metabolismo animal: avanço das pesquisas e perspectivas para o futuro. Rev Nutr. 2008;21(02):195–221.
VIDAL-MARTINS, NETTO, A.S. (Orgs). / Obtenção e processamento do leite e derivados. –- Pirassununga : Faculdade de Zootecnia e Engenharia de Alimentos da Universidade de São Paulo, 2018.
ZABBIA A, Buys EM, de Kock HL. Undesirable Sulphur and carbonyl flavor compounds in UHT milk: A review. Crit Rev Food Sci Nutr. 2012;52(01):21–30.