Mastite é a doença mais comum e onerosa que afeta vacas leiteiras em todo o mundo (Halasa et al., 2007). Define-se a mastite como a inflamação do parênquima mamário, uma reação natural de proteção do organismo em resposta a irritações de qualquer origem. Na maioria dos casos, a mastite é causada por infecções intramamárias, resultantes da entrada de patógenos no úbere.
A mastite pode reduzir significativamente a produção de leite, diminuir a qualidade do leite e aumentar a probabilidade de descarte de animais infectados, gerando custos altos em adição aos custos derivados do uso de medicamentos e serviços veterinários (Seegers et al., 2003; Halasa et al., 2007; Heikkilä et al., 2012). Estimativas indicam que a queda na produção ocorre de 14 a 4 dias antes do início clínico da mastite e pode persistir até 15 a 25 dias após o diagnóstico (Sguizzato et al., 2024).
A presença de patógenos no úbere, com consequente piora da qualidade do leite, pode levar à aplicação de penalidades aos produtores e impactar a lucratividade das fazendas leiteiras. A introdução da tecnologia de PCR revolucionou a área de diagnóstico veterinário e vem ganhando cada vez mais aceitação e espaço no diagnóstico de mastite. Sua alta sensibilidade e capacidade de detectar DNA tornam o PCR útil para identificar infecções causadas por patógenos que podem não crescer bem em condições de cultura convencionais. Porém, isso também levantou, ao longo dos anos, questões sobre como ele se compara à cultura tradicional, se seria sensível “demais” e como os resultados devem ser interpretados na prática.
O manejo da saúde do úbere e a prevenção da mastite dependem de diversos fatores relacionados à vaca, ao manejo e ao rebanho, que são únicos em cada fazenda. A mastite pode ser abordada tanto no nível do rebanho quanto no nível individual da vaca. Por ser uma doença de produção, não é possível eliminá-la completamente, mas excelentes resultados têm sido observados em todo o mundo, independentemente do tamanho da fazenda.
O controle efetivo da mastite nas fazendas exige planejamento, estratégia, monitoramento e liderança — como qualquer problema em qualquer empresa. As medidas de controle mais comuns, adicionalmente às rotinas de manejo, incluem, em geral, ventilação, alimentação, práticas de ordenha, manejo do período de transição e maior foco na imunidade das vacas.
O controle eficaz da mastite depende da identificação precoce e acurada dos agentes causadores, o que permite um tratamento direcionado, reduz a disseminação da infecção e minimiza o uso desnecessário de antimicrobianos. Os dados sobre os patógenos causais nas fazendas devem ser armazenados eletronicamente. Com dados adequados ao longo de um período mais longo, as fazendas conseguem definir seu perfil bacteriano (contagioso, misto ou ambiental) e tratar o problema de forma apropriada, com o apoio de um veterinário especializado em saúde do rebanho.
Detectando a mastite e o agente causador
A contagem de células somáticas (CCS) é um dos indicadores mais utilizados e confiáveis de mastite (Williamson et al., 2022). A CCS mensura o número de macrófagos, neutrófilos e linfócitos (glóbulos brancos), além de células epiteliais mamárias presentes no leite, que aumentam em resposta a uma infecção no úbere. Uma CCS elevada geralmente indica uma infecção subjacente, mas não fornece informação específica sobre o patógeno causador.
Para obter um diagnóstico definitivo, a cultura bacteriana tem sido o padrão-ouro para identificar os patógenos causadores de mastite a partir de amostras de leite coletadas assepticamente dos quartos mamários suspeitos. No entanto, os métodos tradicionais de cultura apresentam limitações, incluindo tempo de resposta lento, sensibilidade reduzida, subjetividade e dificuldades na detecção de certos microrganismos que exigem tempo ou condições especiais de crescimento.
A introdução da tecnologia de PCR revolucionou a área de diagnóstico veterinário e vem ganhando cada vez mais aceitação e espaço no diagnóstico de mastite. O PCR é uma técnica de biologia molecular altamente sensível que amplifica segmentos específicos de DNA para detectar a presença de patógenos em uma amostra de leite. O PCR em tempo real multiplex é uma versão mais avançada da técnica tradicional, permitindo a detecção simultânea de múltiplos patógenos em um único teste (Tang; Stratton, 2013).
Alguns kits voltados à mastite bovina conseguem identificar até 15 dos patógenos mais comuns, incluindo Staphylococcus aureus, Streptococcus uberis, Streptococcus agalactiae e Mycoplasma bovis, além do gene da beta-lactamase, que indica a presença de bactérias resistentes a antimicrobianos beta-lactâmicos. Diferentemente da cultura bacteriana, que depende do crescimento de bactérias viáveis em meio de cultura, o PCR amplifica DNA; por isso, as células bacterianas precisam ser quebradas para a liberação do material genético antes do processo de amplificação (Figura 1). Sua alta sensibilidade e a capacidade de detectar DNA tornam o PCR útil para identificar infecções causadas por patógenos que podem não crescer bem em condições de cultura padrão — o que, ao longo dos anos, também levantou questões sobre como ele se compara à cultura convencional, se seria “sensível demais” e como os resultados devem ser interpretados na prática.
Figura 1. Etapa da extração de DNA dos agentes causadores de mastite, a partir de amostras de leite (Fonte: Clínica do Leite, 2025).
A importância da amostragem adequada
Antes da coleta, é preciso definir o objetivo da coleta: será para monitoramento ou para diagnóstico? Para o rebanho ou para a vaca individual? Diferentes técnicas de amostragem — amostragem do leite do tanque de resfriamento, amostragem composta da vaca e amostragem asséptica por quarto mamário — atendem a propósitos distintos no monitoramento e manejo da saúde do úbere.
1.Amostragem do leite do tanque de resfriamento
A amostragem do leite do tanque (Figura 2) é um método em que se coleta uma amostra diretamente do tanque, englobando o leite de todo o rebanho, pressupondo que o leite de todas as vacas em lactação esteja incluído.
Figura 2. Coleta do leite do tanque (Fonte: Clínica do Leite, 2025).
Quando o PCR é realizado em amostras de leite do tanque, o objetivo geralmente está ligado a programas de erradicação da mastite e à identificação da presença de patógenos contagiosos nos rebanhos. Esse método pode ser particularmente útil para a vigilância em nível de rebanho e para detectar patógenos contagiosos que podem se espalhar de forma agressiva e afetar várias vacas, como Streptococcus agalactiae ou Mycoplasma bovis (Barkema et al., 2009; Timonen et al., 2017; Katholm et al., 2018). Ao testar rotineiramente o leite do tanque por PCR, produtores e veterinários podem monitorar tendências de prevalência de patógenos, detectar precocemente infecções contagiosas emergentes e adotar medidas preventivas antes que ocorra uma disseminação ampla.
2. Amostragem composta da vaca
O objetivo tradicional das amostras compostas é determinar, no nível da vaca, o teor de sólidos do leite e a CCS para programas de melhoramento do rebanho leiteiro (Figura 3). Contudo, elas também podem ser utilizadas para diagnosticar infecções intramamárias subclínicas por meio de testes microbiológicos (Reyher; Dohoo, 2011).
A amostragem composta da vaca envolve coletar leite dos quatro quartos de uma vaca e combiná-lo em uma única amostra, manualmente ou com dispositivo técnico. O uso de amostras não assépticas, em vez de amostras assépticas por quarto, aumenta a sensibilidade do PCR, mantendo a especificidade nos mesmos níveis (Nyman et al., 2016). Amostras compostas podem ser particularmente úteis para triagem de vacas quanto a patógenos contagiosos específicos, como Staphylococcus aureus, Mycoplasma bovis ou Strep. agalactiae, de acordo com as necessidades do rebanho.
No monitoramento por amostras compostas, a coleta é automatizada e não há desinfecção dos quartos. Sistemas automáticos podem levar a um fenômeno chamado “carry-over”. Carry-over refere-se à contaminação não intencional de uma amostra de leite por resíduos de leite da vaca anterior durante a ordenha ou a amostragem. Isso pode ocorrer em sistemas de ordenha automática ou quando se usa equipamento compartilhado, levando à transferência de patógenos entre amostras.
O carry-over pode afetar a acurácia do diagnóstico de mastite, potencialmente causando resultados falso-positivos, pois bactérias de uma vaca podem ser atribuídas erroneamente à amostra de outra. Garantir a limpeza adequada do equipamento e o uso de técnicas assépticas ajuda a minimizar o risco de carry-over. Na triagem de amostras compostas por PCR, a ordem de ordenha e o valor de CT da vaca precedente devem ser considerados no processo diagnóstico (Mahmood et al., 2017).
Figura 3. Coleta de amostras por amostrador (Fonte Clínica do Leite, 2025).
|
|
|
3. Amostragem asséptica por quarto mamário
O objetivo principal da amostragem asséptica por quarto é diagnosticar de forma acurada a mastite clínica e subclínica ao nível de cada quarto (Figura 4). Ela é utilizada quando há suspeita de infecção em um quarto específico com base em sinais clínicos (como CCS elevada ou anormalidades visíveis no leite). Os resultados obtidos com a amostragem por quarto ajudam a decidir se o animal precisa ou não de um antimicrobiano, além de anti-inflamatórios não esteróides. O aspecto mais importante da amostragem asséptica por quarto, além de compor o diagnóstico da vaca individual, é gerar dados confiáveis que formam o perfil bacteriológico do rebanho, orientando o plano de manejo sanitário para as medidas corretas.
Figura 4. Etapas da coleta asséptica: higienização do teto com álcool 70% e coleta da amostra. As luvas devem ser trocadas entre as vacas amostradas. (Fonte: Clínica do Leite, 2025. Vídeo completo de como coletar disponível no link).
|
|
|
Comparando PCR e cultura bacteriana como métodos diagnósticos
A identificação de patógenos causadores de infecções intramamárias pode ser realizada por métodos fenotípicos ou genotípicos. A identificação fenotípica por cultura bacteriana foi considerada por anos o “padrão-ouro”, mas, como afirmam os professores Adkins e Middleton (Adkins; Middleton, 2018), não existe padrão-ouro para o diagnóstico de mastite ou de infecção intramamária. O PCR (reação em cadeia da polimerase) estabelece a identificação genotípica de patógenos-alvo presentes na amostra. A pergunta mais abrangente que diferencia esses dois métodos é: ao usar cultura, perguntamos “O que possivelmente temos na amostra?”, enquanto com PCR perguntamos “O que estamos encontrando?”, já que as possibilidades ficam limitadas aos patógenos-alvo contemplados no kit. Ambos os métodos têm limitações e vantagens.
Tempo de resposta
A cultura bacteriana é demorada: a identificação precisa do patógeno causador geralmente só é possível após 48 horas de incubação e testes diagnósticos adicionais. Para alguns patógenos, como Mycoplasma bovis, a identificação correta requer meios especiais e tempos de incubação de 6 a 10 dias (Maunsell et al., 2011). Kits comerciais de PCR em tempo real multiplex disponíveis atualmente conseguem fornecer resultados em até 3 horas.
Capacidade de detecção, sensibilidade e especificidade
Sensibilidade e especificidade têm sido debatidas: a cultura deixa de encontrar patógenos que deveria detectar ou o PCR produz achados irrelevantes por ser “sensível demais”?
Uma parcela significativa das amostras de casos de mastite clínica e subclínica resulta negativa para crescimento na cultura bacteriana. Estudos mostram de forma consistente que o PCR em tempo real multiplex é um método diagnóstico mais sensível do que a cultura (Tabela 1). Por exemplo, Taponen et al. (2009) demonstraram que o PCR detectou bactérias em 43% dos casos de mastite clínica em que os resultados de cultura foram negativos, enquanto a cultura bacteriana não conseguiu isolar nenhum patógeno (Taponen et al., 2009).
De modo semelhante, Shah et al. (2018) observaram que o PCR detectou bactérias em 100% dos casos de mastite subclínica, enquanto a cultura detectou 90% (Shah et al., 2018). Koskinen et al. (2010) mostraram que o PCR detectou patógenos em 89% dos casos de mastite clínica, em comparação a 77% com a cultura bacteriana (Koskinen et al., 2010). Em um estudo alemão de Spittel e Hoedemaker (2012), o PCR identificou patógenos causadores de mastite em 71% dos casos subclínicos, ao passo que a cultura detectou patógenos em apenas 32% das amostras (Spittel; Hoedemaker, 2012). Amostras de quartos sadios foram positivas para patógenos em 15–28% pelo PCR e em 15–17% pela cultura bacteriana (Tabela 1) (Spittel; Hoedemaker, 2012).
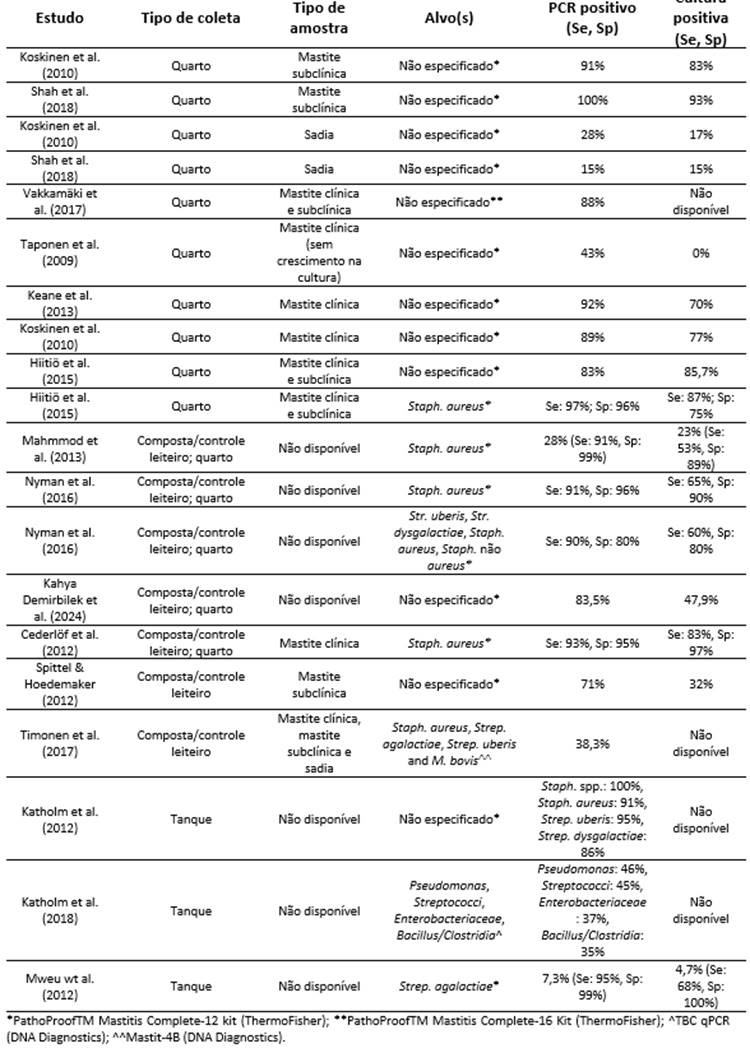
Tabela 1. Capacidade de detecção e/ou sensibilidade (Se) e especificidade (Sp) da cultura bacteriana (BC) e do PCR em diferentes estudos. São apresentados o tipo de coleta de amostra (por quarto mamário, composto por vaca/controle leiteira ou tanque de expansão), o tipo de mastite e os alvos. O alvo “não especificado” significa que todos os alvos do kit utilizado foram detectados. Em alguns estudos, o foco foi encontrar apenas determinados patógenos, mesmo usando kits que incluem outros alvos também.
A sensibilidade e a especificidade do PCR variam de acordo com o valor de corte do CT (cycle threshold) no PCR (Nyman et al., 2016; Hiitiö, 2018), e há indicações de que pode ser viável o ajuste dos valores de corte do CT de forma específica por patógeno, para melhorar a interpretação (Hiitiö, 2018). No entanto, até onde sei, não há publicações sobre isso até o momento. Hiitiö et al. (2018) demonstraram que o PCR pode detectar Staphylococcus spp. vários dias após os resultados de cultura bacteriana terem se tornado negativos.
Isso destaca a importância de interpretar os resultados de PCR no contexto dos sinais clínicos da vaca e dos indicadores de inflamação.
Interpretação dos resultados – contaminação e qualidade da amostra
A exatidão e a confiabilidade dos resultados de PCR, assim como de cultura bacteriana, dependem fortemente da qualidade da amostra de leite coletada. A técnica de coleta asséptica é crucial para evitar contaminação, que pode levar a resultados falso-positivos. Na prática, a contaminação ocorre frequentemente quando bactérias da pele da vaca, do equipamento de ordenha ou do ambiente entram na amostra durante a coleta. Amostras contaminadas podem levar a decisões equivocadas, como tratamentos desnecessários ou descarte de animais. Amostras de boa qualidade para testes por PCR não são um mito. Vakkamäki et al. (2017) publicaram um estudo com mais de 240.000 amostras de rotina, coletadas principalmente por produtores, no qual quase 50% continham apenas um patógeno, 24% continham dois e apenas 13% foram consideradas contaminadas (mais de dois patógenos) (Vakkamäki et al., 2017).
O número de amostras negativas variou de 12% a 18% em dados de amostragem por PCR (Valio Oy, 90–120 mil amostras por ano) (Vakkamäki et al., 2017). Não há consenso sobre os resultados de PCR referentes à contaminação em amostras assépticas por quarto mamário. Sugerimos seguir a definição da cultura bacteriana, considerando como contaminadas as amostras com mais de 2 patógenos; porém, com mais estudos envolvendo valores de corte de CT e a origem dos patógenos, essa definição pode mudar no futuro. Se a amostra contiver mais de três patógenos detectados por PCR, a qualidade dessa amostra é questionável.
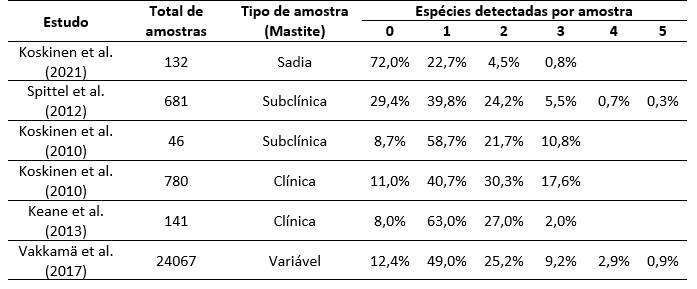
A Tabela 2 mostra a qualidade das amostras quanto ao número de patógenos detectados por amostra em diferentes estudos. A tabela apresentada é da Tese de Doutorado de Hiitiö (2018).
Tabela 2. Porcentagem de amostras em que nenhum (0) patógeno-alvo (DNA) foi detectado e de amostras contendo DNA-alvo de 1 a 5 espécies diferentes por amostra de leite de quarto coletado assepticamente, analisadas por PCR em tempo real (kit PathoProof™ Complete-12 ou Complete-16).
Momento da coleta
Além da técnica asséptica, o momento da coleta é crítico para resultados acurados. O PCR é mais confiável quando as amostras são coletadas durante a fase aguda da inflamação, quando a carga bacteriana é maior. A interpretação é mais fácil quando um único patógeno domina a amostra (>99%) e o valor de CT é baixo, indicando um forte sinal de DNA (Hittiö, 2018).
Resultados negativos
Um dos principais desafios dos métodos baseados em cultura é que podem resultar em alta proporção de resultados negativos.
studos (Sears et al., 2003; Rainard et al., 2006; Koivula et al., 2007; Walker et al., 2010) relataram que até 27% dos casos de mastite clínica e mais de 40% dos casos subclínicos podem apresentar cultura negativa, apesar de sinais claros de inflamação, como alterações visíveis no leite e CCS elevada, respectivamente.
- Baixa carga bacteriana: O número de bactérias na amostra pode ser muito baixo para detecção por cultura, especialmente em infecções subclínicas ou nos estágios iniciais da infecção.
- Curta duração da infecção: Infecções transitórias ou recentemente eliminadas pelo sistema imune da vaca podem resultar em cultura negativa.
- Compostos inibitórios: O leite de vacas com mastite contém diversos compostos, como leucócitos e proteínas antimicrobianas, que podem inibir o crescimento bacteriano em cultura. Adicionalmente, em amostras coletadas para acompanhar a cura, antimicrobianos podem estar presentes em níveis que inibem o crescimento.
- Coleta e armazenamento: O tempo e o manuseio entre a coleta e a realização da cultura também podem afetar a viabilidade bacteriana, levando a resultados falso-negativos.
- Processos laboratoriais: O processo laboratorial não é realizado conforme o procedimento operacional (NMC 2017). Por exemplo, manuseio inadequado, tempos de incubação menores que o necessário. Outro motivo seriam placas de ágar com defeito.
- Interpretação equivocada: Placa descartada antes de haver crescimento visível.
- A amostra não contém patógenos viáveis capazes de crescer no ágar.
Resultados negativos no PCR podem ocorrer devido a:
- O agente causal não está entre os incluídos no kit utilizado.
- Falha no processo de PCR: Problemas técnicos; reagentes defeituosos.
- O DNA se perdeu/dissolveu na amostra por algum motivo; por exemplo, quantidade excessiva de desinfetantes durante a coleta.
- A amostra não contém DNA de patógenos.
- Quantidade muito baixa de DNA do patógeno-alvo na amostra: A amplificação bem-sucedida no PCR geralmente requer apenas 5 cópias do alvo (Klein, 2002).
Questões de subjetividade
O processo de cultura envolve o crescimento de bactérias de amostras de leite em placas de ágar, e os resultados são interpretados com base na aparência das colônias bacterianas. Isso introduz vários pontos potenciais de subjetividade, como a avaliação da amostra de leite antes da cultura, a identificação das colônias por seu tamanho, forma, cor e padrão de crescimento, além de testes laboratoriais adicionais. Trata-se de um processo altamente subjetivo, apesar das diretrizes e padrões de prática, tanto para laboratórios quanto para métodos de cultura (ISO/IEC 17025, 2017; Middleton et al., 2017).
O grau de subjetividade, tanto na interpretação quanto no manuseio, foi demonstrado em estudos de proficiência (Pitkälä et al., 2005; Karlsmose et al., 2013). Noruega e Suécia realizam rotineiramente testes de proficiência próprios e os resultados estão alinhados com os publicados.
Na Suécia, 39% dos 112 laboratórios obtiveram desempenho insuficiente na interpretação de cultura bacteriana (notas de 1 a 5/10, sendo 10 a identificação correta de todos) (NJK Nordic Mastitis Seminar 2024). A variabilidade interpretativa inerente à cultura bacteriana significa que os resultados diferem conforme a habilidade e a experiência do microbiologista/veterinário e exigem julgamento especializado.
Há também variação nos limites de detecção para infecção intramamária na cultura, de modo semelhante ao PCR com pontos de corte de CT. A decisão sobre o que constitui uma contagem bacteriana significativa para infecção intramamária (unidades formadoras de colônia por mililitro, ufc/ml) pode variar entre laboratórios e também diferiu entre os estudos, de 100 ufc/mL a 500 ufc/mL, e em alguns casos variou de acordo com o patógeno (Pitkälä et al., 2004; Østerås et al., 2006; Bradley et al., 2007).
O diagnóstico por PCR é considerado um método objetivo em termos do próprio processo. Após a coleta e o manuseio manual da amostra antes da amplificação por PCR, o processo de PCR torna-se mais objetivo em condições laboratoriais, com calibrações adequadas e inclusão de controles negativos em cada análise (Tang; Stratton, 2013).
A interpretação das curvas de amplificação é automatizada, e um software gera os resultados. Isso torna o processo mais objetivo, mas a origem do patógeno (especialmente os ambientais) permanece incerta se a amostra não for coletada de forma asséptica. As diretrizes de interpretação da NMC (2019) afirmam que, devido ao alto risco de contaminação e à dificuldade de interpretar corretamente a presença de bactérias ambientais, amostras de controle leiteiro podem não ser recomendadas para uso com PCR.
Benefícios e limitações do PCR no diagnóstico de mastite
O PCR em tempo real multiplex apresenta várias claras vantagens em relação aos métodos tradicionais baseados em cultura para o diagnóstico de mastite bovina. De acordo com o National Mastitis Council (2019), as técnicas de PCR podem ser uma alternativa viável à cultura bacteriana clássica no diagnóstico de infecções intramamárias que causam mastite clínica e subclínica quando se utilizam amostras assépticas por quarto mamário ou amostras compostas. O PCR pode ser mais sensível, mais rápido e não requer, necessariamente, transporte refrigerado das amostras.
Benefícios do diagnóstico por PCR:
- Rapidez:
- O PCR pode fornecer resultados diagnósticos em questão de horas, permitindo decisões terapêuticas mais ágeis.
- A rapidez é especialmente crítica em casos de mastite clínica, nos quais a intervenção oportuna é essencial para evitar a disseminação da infecção e minimizar perdas de produção.
- Para aproveitar o benefício da velocidade, o volume de testes deve ser suficiente e o PCR deve ser realizado diariamente.
- O PCR pode fornecer resultados diagnósticos em questão de horas, permitindo decisões terapêuticas mais ágeis.
- Alta sensibilidade
- O PCR é altamente sensível, capaz de detectar pequenas quantidades de DNA bacteriano em amostras de leite. Isso é particularmente vantajoso no diagnóstico de mastite subclínica, em que a carga bacteriana pode ser baixa demais para ser detectada por métodos de cultura tradicionais.
- A capacidade de identificar infecções em estágios iniciais permite um manejo mais proativo da saúde do úbere.
- Detecção de bactérias mortas também pode ser considerada uma vantagem
- É possível utilizar conservantes na amostra de leite. Isso “congela” a situação no momento da coleta, sem o risco de, por exemplo, Escherichia coli crescer acima de outros patógenos durante o transporte e enviesar os resultados.
- Útil quando, por algum motivo, bactérias viáveis não são detectáveis por cultura.
- Ampla aplicação
- Ferramenta útil para vigilância em nível de rebanho e monitoramento da saúde do úbere por meio de amostras de leite do tanque e amostras compostas da vaca ou de controle leiteiro. Por exemplo, a testagem regular de amostras de leite do tanque pode ajudar a detectar precocemente patógenos contagiosos como Mycoplasma bovis, permitindo intervenção rápida para evitar surtos em todo o rebanho.
Encontrar DNA em vez de células viáveis — como interpretar?
Embora o PCR seja sensível e acurado, há um debate sobre a relevância de certos achados. Um dos principais desafios do PCR é que ele não distingue entre patógenos vivos e mortos. Isso pode levar a resultados falso-positivos, especialmente quando a infecção já foi eliminada, mas o DNA bacteriano permanece no úbere. Ao mesmo tempo, é importante entender que o resultado de uma amostra de leite é apenas uma parte — embora importante — do diagnóstico de mastite.
Valores de CT, isoladamente, não fornecem uma compreensão completa da gravidade da infecção nem do estado clínico da vaca. Ao tomar decisões terapêuticas com base nos resultados de PCR, os veterinários devem considerar o histórico da vaca, os sinais clínicos, a CCS e outros fatores. Também devem comparar os resultados diagnósticos com a severidade dos sintomas clínicos da vaca. Por exemplo, se não há sinais de mastite clínica e o resultado é “alta quantidade de E. coli”, isso pode indicar contaminação por fezes na amostra.
Isso é extremamente importante quando se considera a administração de antimicrobianos, pois o PCR pode continuar detectando DNA bacteriano morto. Nessas situações, é essencial interpretar os resultados de PCR em conjunto com outras informações diagnósticas, como o histórico clínico da vaca, a CCS e a presença de sinais visíveis de mastite. A exatidão e a confiabilidade dos resultados de PCR dependem fortemente da qualidade da amostra de leite coletada. Técnicas assépticas de coleta são cruciais para evitar contaminação, que pode levar a falso-positivos. Na prática, a contaminação frequentemente ocorre quando bactérias da pele da vaca, do equipamento de ordenha ou do ambiente entram na amostra durante a coleta.
Além das técnicas assépticas, o momento da coleta é crítico para obter resultados acurados no PCR. Pesquisas mostram que o PCR é mais confiável quando as amostras são coletadas durante a fase aguda da inflamação, quando a carga bacteriana está mais alta. Hiitiö et al. (2018) demonstraram que o PCR pode detectar Staphylococcus spp. vários dias após os resultados de cultura bacteriana terem se tornado negativos. Isso destaca a importância de interpretar os resultados de PCR no contexto dos sinais clínicos da vaca e dos indicadores de inflamação.
Interpretando resultados de PCR: o papel dos valores de CT
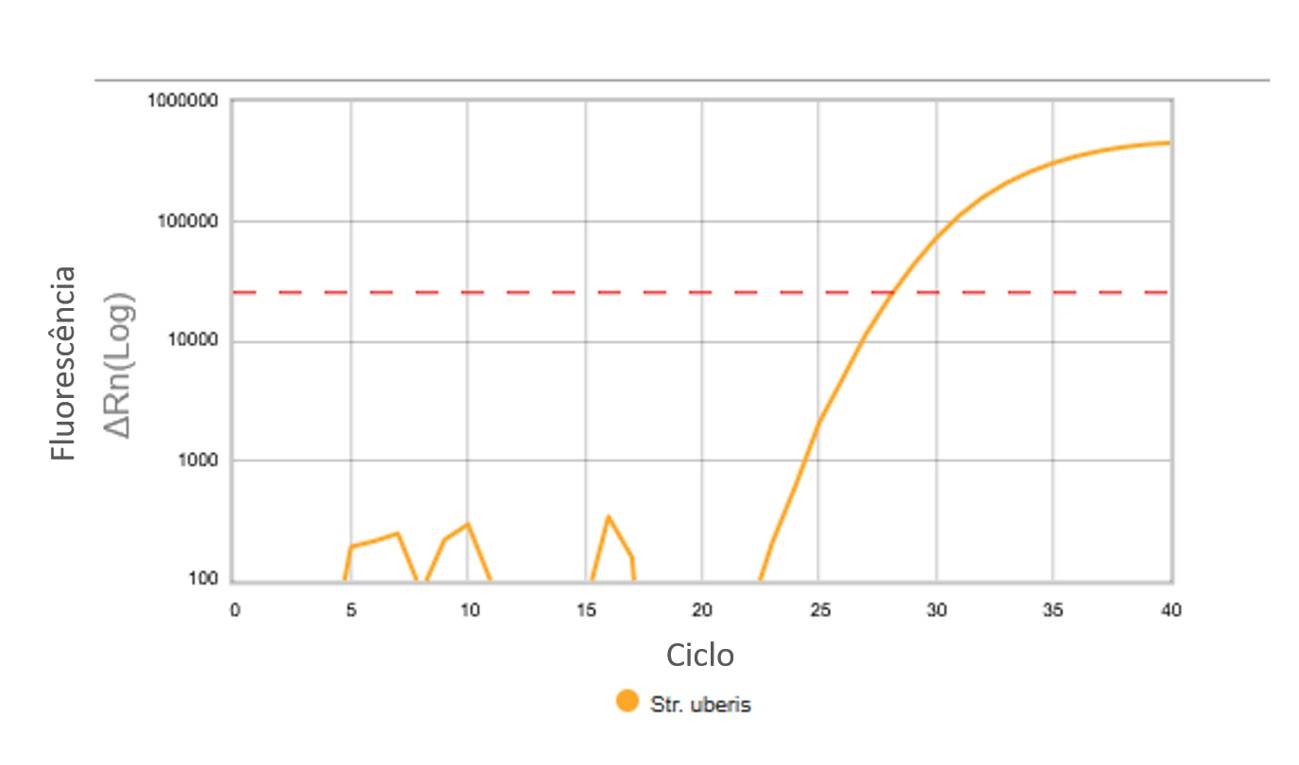
Os resultados de PCR são frequentemente reportados como valores de cycle threshold (CT), que indicam o número de ciclos necessários para detectar o DNA-alvo na amostra (Figura 5). O valor de CT é inversamente proporcional à quantidade de DNA bacteriano na amostra — CTs mais baixos correspondem a cargas bacterianas mais altas, enquanto CTs mais altos indicam menores quantidades de DNA. A maioria dos ensaios comerciais de PCR utiliza um valor de corte de 37 ciclos; qualquer resultado detectado após 37 ciclos é considerado negativo ou inconclusivo.
Figura 5. Curva de amplificação do DNA de Streptococcus uberis em ensaio de PCR. A linha pontilhada indica o limiar para indicar a presença de DNA na amostra. Nesse ensaio, o valor de CT foi igual a 28, isto é, foram necessários 28 ciclos para detectar o DNA alvo (Fonte: Clínica do Leite, 2025).
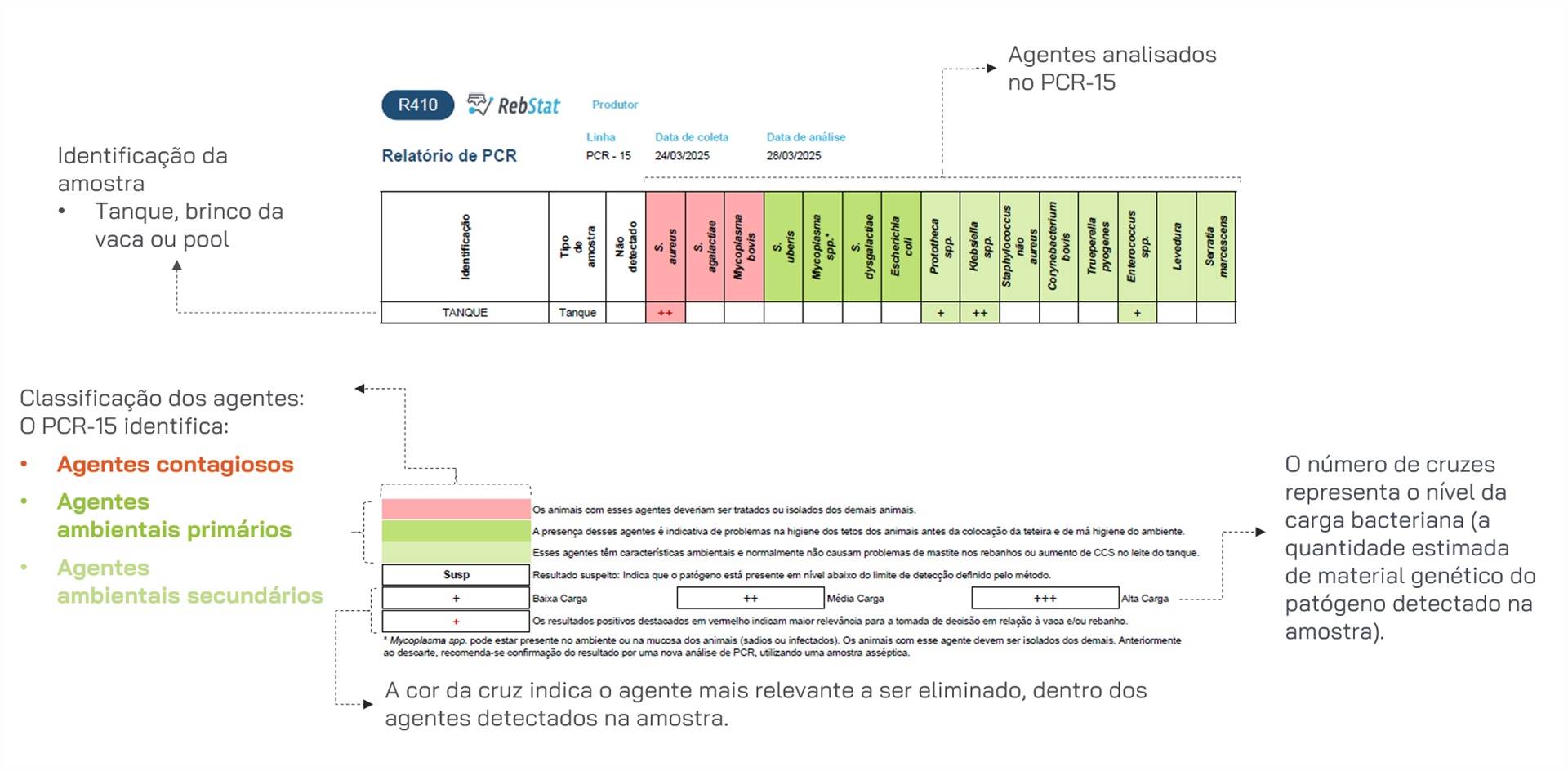
Os valores de CT são essenciais para interpretar a gravidade da infecção. Por exemplo, um CT baixo (por exemplo, menor do que 25) sugere alta carga bacteriana e infecção ativa, ao passo que um CT alto (por exemplo, maior do que 37) pode indicar contaminação ou presença de bactérias mortas. Alguns laboratórios reportam os resultados de PCR como carga bacteriana alta (+++), moderada (++) ou baixa (+) com base no CT (Figura 6).
Os sinais de “+” e suas faixas de CT correspondentes vêm mudando ao longo dos anos, à medida que novas informações surgem. Certos ensaios de PCR em tempo real reportam Streptococcus uberis com um “+” em CT de 28,1, enquanto esse mesmo valor já foi indicado como “++”.
O mesmo se aplica a leveduras. Esse resultado não está relacionado aos sintomas do animal. Quatorze por cento dos veterinários finlandeses declararam considerar os valores de CT muito úteis para avaliar a confiabilidade dos resultados de PCR, e 21% afirmaram que os utilizariam se fossem fornecidos (Hiitiö, 2018). A escala de “+” ou “++”, considerando a quantidade de DNA na amostra, é ampla. Sem os valores de CT, podemos ter uma situação em que o resultado é “baixa quantidade”, mas o CT está próximo de “intermediário”, o que pode enviesar nossa interpretação.
Portanto, eu recomendaria que todos os laboratórios reportassem os valores de CT reais juntamente com os sinais de “+”. Contudo, é importante lembrar que os valores de CT, por si sós, não fornecem um quadro completo da possível infecção. Os resultados devem ser interpretados em conjunto com outros dados clínicos e diagnósticos, como a CCS da vaca, sinais clínicos e histórico de tratamentos.
Figura 6. Formato do relatório com os resultados de PCR da Clínica do Leite. Resultados são apresentados de acordo com a carga bacteriana detectada para o patógeno: carga bacteriana baixa (“+”), carga bacteriana média (“++”) e carga bacteriana alta (“+++”). Importante ressaltar que a detecção de Staphylococcus aureus, independente da carga, é relevante, visto que a quantidade secretada desse patógeno varia ao longo do dia (Fonte: Clínica do Leite, 2025).
Nos casos em que os resultados do PCR não estão alinhados com os sintomas clínicos ou com a CCS, pode ser necessário repetir a análise da amostra ou realizar uma cultura bacteriana para confirmar o diagnóstico. Isso é particularmente importante quando o PCR detecta múltiplos patógenos na mesma amostra, pois coinfecções podem complicar as decisões terapêuticas.
Experiência prática da Finlândia
Nosso principal laboratório para diagnóstico de mastite pertence à Valio Oy, a maior indústria láctea da Finlândia, que atende 80% das fazendas. A Valio substituiu a cultura bacteriana pelo PCR em junho de 2010, mudando o diagnóstico finlandês da noite para o dia. Desde 2010, o PCR é uma ferramenta de rotina.
Mais de 130.000 amostras são analisadas por PCR todos os anos, enquanto o número de amostras para cultura é de cerca de 2.000. A mudança foi rápida, e a maior dificuldade decorreu da falta de diretrizes de interpretação. A introdução do PCR no mercado gerou receios de que o uso de antibióticos dispararia. No entanto, a tendência foi exatamente a oposta, como mostra o relatório da Fimea sobre monitoramento e consumo de antimicrobianos veterinários na Finlândia: FINRES-VET 2022 (Finnish Food Authority, 2022).
Esse sucesso se deve a colegas e produtores: a mentalidade é buscar um resultado confiável a partir de amostra asséptica, esperando um desfecho em que possamos manejar com tratamentos de suporte e anti-inflamatórios não esteróides, sem antimicrobianos caros. A saúde do úbere passou a ser considerada de forma mais holística, com foco na prevenção. O número de tratamentos desnecessários ou “por precaução” parece ter diminuído. O PCR, como outros testes, sempre tem seus desafios e pontos a desenvolver.
Ainda são necessárias mais pesquisas. Na minha opinião, o uso rotineiro do PCR se justifica em termos de logística, rapidez e objetividade. A forma finlandesa de coletar amostras e compilar os resultados em um formato de fácil uso como ferramenta para a saúde do úbere é única no mundo. Isso oferece uma excelente base para continuar trabalhando em benefício dos produtores e da produção de leite de alta qualidade.
A tese “Multiplex Real-Time PCR in bovine mastitis diagnostics” (2018) está disponível na íntegra aqui.
A versão original deste artigo está disponível na M2-magazine (link aqui). Para mais informações sobre a análise de PCR, como coletar as amostras e solicitar a análise à Clínica do Leite, acesse o nosso guia com informações sobre esse serviço no link.
Redigido por Dra. Heidi Hiitö (Pinehill Goblin Oy Consulting)
Traduzido por Juliana Petrini e Paulo Fernando Machado
Referências bibliográficas:
Adkins, P. R. F. & Middleton, J. R. (2018) Methods for Diagnosing Mastitis. Veterinary Clinics of North America: Food Animal Practice, 34, 479–491.
Barkema, H. W., Green, M. J., Bradley, A. J. & Zadoks, R. N. (2009). Invited review: The role of contagious disease in udder health. Journal of Dairy Science, 92, 4717–4729.
Bradley, A. J., Leach, K. A., Breen, J. E., Green, L. E. & Green, M. J. (2007). Survey of the incidence and aetiology of mastitis on dairy farms in England and Wales. Veterinary Record, 160, 253–258.
Cederlöf, S. E., Toft, N., Aalbaek, B. & Klaas, I. C. (2012). Latent class analysis of the diagnostic characteristics of PCR and conventional bacteriological culture in diagnosing intramammary infections caused by Staphylococcus aureus in dairy cows at dry off. Acta Veterinaria Scandinavica, 54, 65.
Finnish Food Authority. FINRES-Vet 2022 - Finnish veterinary antimicrobial resistance monitoring and consumption of antimicrobial agents. Disponível em: < https://helda.helsinki.fi/items/0e5e18e3-3ef8-4e2c-b2aa-abff217b410e>.
Halasa, T., Huijps, K., Østerås, O. & Hogeveen, H. (2007). Economic effects of bovine mastitis and mastitis management: A review. Veterinary Quarterly, 29, 18–31.
Heikkilä, A.-M., Nousiainen, J. I. & Pyörälä, S. (2012). Costs of clinical mastitis with special reference to premature culling. Journal of Dairy Science, 95, 139–150.
Hiitiö, H. (2018). Multiplex Real-Time PCR in Bovine Mastitis Diagnostics. Disponível em: < https://helda.helsinki.fi/server/api/core/bitstreams/9e406d43-e2c0-4cec-8abb-bcbc30daaa87/content>.
Hiitiö, H., Riva, R., Autio, T., Pohjanvirta, T., Holopainen, J., Pyörälä, S. & Pelkonen, S. (2015). Performance of a real-time PCR assay in routine bovine mastitis diagnostics compared with in-depth conventional culture. Journal of Dairy Research, 82, 200–208.
ISO/IEC 17025. (2017) General requirements for the competence of testing and calibration laboratories.
Kahya Demirbilek, S., Yildiz, M., Akkoç, A., Mutlu, A. M., Ardiçli, O., Aner, H. (2024). Comparison of bacteriological culture method and multiplex real-time PCR for detection of mastitis. Research in Veterinary Science, 172, 105237.
Karlsmose, S., Kunstmann, L., Rundsten, C. F., Krogh, K., Larsen, H. K. D., Jensen, A. B., Aarestrup, F. M., Hendriksen, R. S. (2013). External quality assurance system (EQAS) for identification of mastitis pathogens in Denmark from 2006 to 2011. Preventive Veterinary Medicine, 109, 271–277.
Katholm, J., Bennedsgaard, T. W., Koskinen, M. T. & Rattenborg, E. (2012). Quality of bulk tank milk samples from Danish dairy herds based on real-time polymerase chain reaction identification of mastitis pathogens. Journal of Dairy Science, 95, 5702–5708.
Katholm, J., Olesen, L. T., Petersen, A. & Sigurdsson, S. (2018). Evaluation of a new qPCR test to identify the organisms causing high total bacterial count in bulk tank milk. Journal of Integrative Agriculture, 17, 1241–1245.
Keane, O. M., Budd, K. E., Flynn, J. & McCoy, F. (2013). Increased detection of mastitis pathogens by real-time PCR compared to bacterial culture. Veterinary Record, 173, 268–268.
Klein, D. Quantification using real-time PCR technology: applications and limitations. (2002). Trends in Molecular Medicine, 8, 257–260.
Koivula, M., Pitkälä, A., Pyörälä, S. & Mäntysaari, E. A. (2007). Distribution of bacteria and seasonal and regional effects in a new database for mastitis pathogens in Finland. Acta Agriculturae Scandinavica, Section A - Animal Science 57, 89–96.
Koskinen, M. T., Wellenberg, G. J., Sampimon, O. C., Holopainen, J., Rothkamp, A., Salmikivi, L., van Haeringen, W. A., Lam, T. J. G. M., Pyörälä, S. (2010). Field comparison of real-time polymerase chain reaction and bacterial culture for identification of bovine mastitis bacteria. Journal of Dairy Science, 93, 5707–5715.
Mahmmod, Y. S., Klaas, I. C. & Enevoldsen, C. (2017). DNA carryover in milk samples from routine milk recording used for PCR-based diagnosis of bovine Staphylococcus aureus mastitis. Journal of Dairy Science, 100, 5709–5716.
Mahmmod, Y. S., Toft, N., Katholm, J., Grønbæk, C. & Klaas, I. C. (2013). Bayesian estimation of test characteristics of real-time PCR, bacteriological culture and California mastitis test for diagnosis of intramammary infections with Staphylococcus aureus in dairy cattle at routine milk recordings. Preventive Veterinary Medicine, 112, 309–317.
Maunsell, F. P., Woolums, A. R., Francoz, D., Rosenbusch, R. F., Step, D. L., Wilson, D. J. & Janzen, E. D. (2011). Mycoplasma bovis infections in cattle. Veterinary Internal Medicine, 25, 772–783.
Middleton, J. R., L. K., Fox, G., Pighetti, & and C. Petersson-Wolfe. (2017). Laboratory Handbook on Bovine Mastitis. 3rd Ed. National Mastitis Council, Inc., Minnesota, USA.
Mweu, M. M., Toft, N., Katholm, J. & Nielsen, S. S. (2012). Evaluation of two herd-level diagnostic tests for Streptococcus agalactiae using a latent class approach. Veterinary Microbiology, 159, 181–186.
Nyman, A.-K., Persson Waller, K., Emanuelson, U. & Frössling, J. (2016). Sensitivity and specificity of PCR analysis and bacteriological culture of milk samples for identification of intramammary infections in dairy cows using latent class analysis. Preventive Veterinary Medicine, 135, 123–131
Østerås, O., Sølverød, L. & Reksen, O. (2006). Milk culture results in a large Norwegian survey—Effects of season, parity, days in milk, resistance, and clustering. Journal of Dairy Science, 89, 1010–1023.
Pitkälä, A., Gindonis, V., Wallin, H. & Honkanen-Buzalski, T. (2005). Interlaboratory proficiency testing as a tool for improving performance in laboratories diagnosing bovine mastitis. Journal Dairy Science, 88, 553–559.
Pitkälä, A., Haveri, M., Pyörälä, S., Myllys, V. & Honkanen-Buzalski, T. (2004). Bovine Mastitis in Finland 2001—Prevalence, distribution of bacteria, and antimicrobial resistance. Journal of Dairy Science, 87, 2433–2441.
Rainard, P. & Riollet, C. (2006). Innate immunity of the bovine mammary gland. Veterinary Research, 37, 369–400.
Reyher, K. K. & Dohoo, I. R. Diagnosing intramammary infections: Evaluation of composite milk samples to detect intramammary infections. Journal of Dairy Science 94, 3387–3396 (2011).
Sears, P. M. & McCarthy, K. K. (2003). Diagnosis of mastitis for therapy decisions. Veterinary Clinics of North America: Food Animal Practice, 19, 93–108.
Seegers, H., Fourichon, C. & Beaudeau, F. (2003). Production effects related to mastitis and mastitis economics in dairy cattle herds. Veterinary Research, 34, 475–491.
Sguizzato, A. L. L., Silva, T.E., Chagas, J.C.C., Argüelo, A.M., Gonçalves, N.M. & Marcondes, M.I. (2024). Understanding the dynamics of mastitis in milk yield: decoding onset and recovery patterns in response to mastitis occurrence. JDS Communications, 5(6), 669-673.
Shah, K., Nauriyal, D. & Joshi, C. (2018). Real-time PCR based assay offers high resolution in detecting bacterial species from bovine sub-clinical mastitis for prudent antimicrobial treatment. Journal of Pure and Applied Microbiology, 12, 887–895.
Spittel, S. & Hoedemaker, M. (2012). Mastitis diagnosis in dairy cows using PathoProof real-time polymerase chain reaction assay in comparison with conventional bacterial culture in a Northern German field study. Berliner und Münchener tierärztliche Wochenschrift, 125, 494–502.
Tang, Y-W. & Stratton, C.W. (2013). Advanced Techniques in Diagnostic Microbiology. Springer US, Boston, MA.
Taponen, S., Salmikivi, L., Simojoki, H., Koskinen, M. T. & Pyörälä, S. (2009). Real-time polymerase chain reaction-based identification of bacteria in milk samples from bovine clinical mastitis with no growth in conventional culturing. Journal of Dairy Science, 92, 2610–2617.
Timonen, A. A. E., Katholm, J., Petersen, A., Mõtus, K. & Kalmus, P. (2017). Within-herd prevalence of intramammary infection caused by Mycoplasma bovis and associations between cow udder health, milk yield, and composition. Journal of Dairy Science, 100, 6554–6561.
Vakkamäki, J., Taponen, S., Heikkilä, A.-M. & Pyörälä, S. (2017). Bacteriological etiology and treatment of mastitis in Finnish dairy herds. Acta Veterinaria Scandinavica, 59, 33.
Walker, J. B., Rajala-Schultz, P. J. & DeGraves, F. J. (2010). The effect of inoculum volume on the microbiologic detection of naturally occurring Staphylococcus aureus intramammary infections. Journal of Veterinary Diagnostic Investigation, 22, 720–724.
Williamson, J., Callaway, T., Rollin, E. & Ryman, V. (2022). Association of milk somatic cell count with bacteriological cure of intramammary infection—A Review. Agriculture, 12, 1437.