As caseínas são as principais proteínas encontradas no leite de vaca, compondo 80% do conteúdo proteico e constituída por quatro principais moléculas de caseína: αS1, αS2, β e κ-caseínas. A β-caseína é a mais hidrofóbica (insolúvel em água, mas solúvel em lipídeos e solventes orgânicos) das caseínas, sendo fortemente anfifílica (Farrell Junior, 2011). As duas formas mais comuns de proteína β-caseína são A1 e A2 (Farrell et al., 2004; Pal et al., 2015; Shashank et al., 2018).
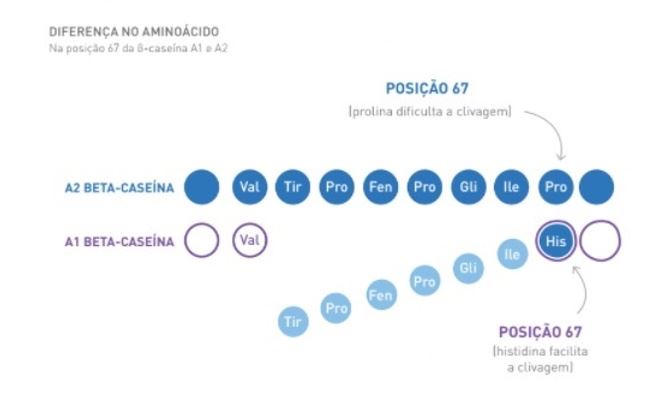
O leite A1 é semelhante ao leite A2, em termos nutricionais, em relação às proteínas, gorduras, carboidratos, vitaminas e minerais. A única diferença entre A1 e A2 β-caseína está no tipo de aminoácidos na 67 posição, sendo a histidina no leite A1 e prolina para A2 (Kaskous et al., 2020), como observado na Figura abaixo.
Fonte: adaptado de Revista Leite Integral (2019).
Diferente do leite A1, o leite A2 é semelhante ao leite humano e pode ser facilmente absorvido pelo corpo, o que leva ao alívio dos sintomas de intolerância à lactose, como distensão abdominal, ruído intestinal e desconforto digestivo (Jianqin et al., 2015; He et al., 2017; Milan et al., 2020).
Os produtores de leite em todo o mundo são incentivados a produzir leite A2 para atender à crescente demanda do consumidor (Bodnár et al., 2018; Bentivoglio et al., 2020). No entanto, a falta de uma técnica eficaz para realizar a discriminação rápida do leite A1 e A2 é um grande desafio.
Atualmente, o teste genético é um dos métodos mais comuns e precisos para identificar genótipos de β-caseína. Contudo, o teste leva muito tempo para ser realizado, além de oneroso e não conseguir suprir aos requisitos de produção em larga escala dos laticínios. Por este motivo, faz-se necessário o desenvolvimento de um método que seja rápido e de baixo valor para que indústrias com grandes demandas consigam identificar essa categoria de leite.
A espectroscopia de infravermelho médio (MIR), por entregar respostas rápidas, exigir pouca manipulação e preparo de amostra, além de apresentar alta precisão e facilidade de aplicação no campo, é utilizado para a obtenção de informações espectrais de uma amostra e é amplamente empregada no controle de qualidade nas indústrias de produtos lácteos (De Marchi et al., 2009) e na detecção de conteúdo de caseína (Bonfatti et al., 2011; McDermott et al., 2016; Ma et al., 2021).
Na região do infravermelho médio, quando a radiação eletromagnética atravessa a amostra, as ligações das moléculas se movimentando de forma vibracional ou rotacional, envolvendo uma incorporação relevante da energia fornecida. Com base nessa energia fornecida e no montante absorvido, juntamente da utilização de dados matemáticos, é possível determinar a composição química da amostra e as características necessárias (De Marchi et al., 2014).
Estudos realizados por Gottardo et al.(2015) e Niero et al. (2016) indicaram que no modelo de previsão de acidez titulável, conteúdo de cálcio e de proteína do leite, se aplicado o procedimento de eliminação de variável não informativa (UVE) para selecionar as variáveis de número de onda mais informativas — eliminando os comprimentos de onda irrelevantes e selecionando as variáveis espectrais MIR mais informativas —, é possível reduzir o tempo de execução e a melhoria da precisão de predição do modelo.
Portanto, por ser um método rápido, barato e preciso, a utilização da técnica de espectrometria do infravermelho médio pode se tornar uma opção para a avaliação de características da composição e fenotípicas do leite.
Leia também:
Referências
Farrell Jr, H. M., Jimenez-Flores, R., Bleck, G. T., Brown, E. M., Butler, J. E., Creamer, L. K., ... & Swaisgood, H. E. (2004). Nomenclature of the proteins of cows’ milk—Sixth revision. Journal of dairy science, 87(6), 1641-1674.
Shashank, C. G., Puri, R. K., Gandhi, G., Kaur, T., & Kushwaha, M. K. M. (2018). A1 and A2 beta casein: Twin faces of milk. J. Pharmacogn. Phytochem, 7, 221-224.
Pal, S., Woodford, K., Kukuljan, S., & Ho, S. (2015). Milk intolerance, beta-casein and lactose. Nutrients, 7(9), 7285-7297.
Kaskous, S. (2020). A1-and A2-milk and their effect on human health. J. Food Eng. Technol, 9, 15-21.
Flávia Fontes. Tudo que você precisa saber sobre leite A2. Revista leite integral, publicado em 14 de Janeiro de 2019. Acesso em 02 de Janeiro de 2022. https://www.revistaleiteintegral.com.br/noticia/tudo-o-que-voce-precisa-saber-sobre-leite-a2
Jianqin, S., Leiming, X., Lu, X., Yelland, G. W., Ni, J., & Clarke, A. J. (2015). Effects of milk containing only A2 beta casein versus milk containing both A1 and A2 beta casein proteins on gastrointestinal physiology, symptoms of discomfort, and cognitive behavior of people with self-reported intolerance to traditional cows’ milk. Nutrition journal, 15(1), 1-16.
He, Mei, et al. Effects of cow’s milk beta-casein variants on symptoms of milk intolerance in Chinese adults: a multicentre, randomised controlled study. Nutrition journal 16.1 (2017): 1-12.
Milan, A. M., Shrestha, A., Karlström, H. J., Martinsson, J. A., Nilsson, N. J., Perry, J. K., ... & Cameron-Smith, D. (2020). Comparison of the impact of bovine milk β-casein variants on digestive comfort in females self-reporting dairy intolerance: a randomized controlled trial. The American journal of clinical nutrition, 111(1), 149-160.
Bodnár, Á., Hajzsér, A., Egerszegi, I., Póti, P., Kuchtik, J., & Pajor, F. (2018). A2 milk and its importance in dairy production and global market. Animal Welfare, Etológia és Tartástechnológia, 14(1), 1-7.
Bentivoglio, D., Finco, A., Bucci, G., & Staffolani, G. (2020). Is There a Promising Market for the A2 Milk? Analysis of Italian Consumer Preferences. Sustainability, 12(17), 6763.
De Marchi, M., Bonfatti, V., Cecchinato, A., Di Martino, G., & Carnier, P. (2009). Prediction of protein composition of individual cow milk using mid-infrared spectroscopy. Italian Journal of Animal Science, 8(sup2), 399-401.
Bonfatti, V., Di Martino, G., & Carnier, P. (2011). Effectiveness of mid-infrared spectroscopy for the prediction of detailed protein composition and contents of protein genetic variants of individual milk of Simmental cows. Journal of dairy science, 94(12), 5776-5785.
McDermott, A., Visentin, G., De Marchi, M., Berry, D. P., Fenelon, M. A., O’connor, P. M., ... & McParland, S. (2016). Prediction of individual milk proteins including free amino acids in bovine milk using mid-infrared spectroscopy and their correlations with milk processing characteristics. Journal of Dairy Science, 99(4), 3171-3182.
Ma, Z., Wang, F., Wang, W., Zhong, Y., & Dai, H. (2021). Deep learning for in vivo near-infrared imaging. Proceedings of the National Academy of Sciences, 118(1).
De Marchi, M., Toffanin, V., Cassandro, M., & Penasa, M. (2014). Invited review: Mid-infrared spectroscopy as phenotyping tool for milk traits. Journal of Dairy Science, 97(3), 1171-1186.
Gottardo, P., De Marchi, M., Cassandro, M., & Penasa, M. (2015). Improving the accuracy of mid-infrared prediction models by selecting the most informative wavelengths. Journal of dairy science, 98(6), 4168-4173.
Niero, G., Penasa, M., Gottardo, P., Cassandro, M., & De Marchi, M. (2016). Selecting the most informative mid-infrared spectra wavenumbers to improve the accuracy of prediction models for detailed milk protein content. Journal of dairy science, 99(3), 1853-1858.
*Fonte da foto do artigo: Freepik