Bruno Delphino Medrado
Médico Veterinário – Instituto Federal Baiano – Campus Santa Inês
Doutorando – PPGCAT – UFBA
Luís Fernando Batista Pinto
Professor Dr. – Programa de Pós-Graduação em Ciência Animal nos Trópicos – Universidade Federal da Bahia
Introdução
As infecções parasitárias gastrintestinais estão entre os principais problemas sanitários que afetam animais em pastejo ao redor do mundo. No Brasil, Haemonchus contortus, Cooperia sp., Trichostrongylus sp., Moniezia expansa e Oesophagostomun sp. são as espécies mais comumente encontradas (Cenci et al., 2007) e os níveis produtivos podem ser bastante reduzidos pelas verminoses e, se não forem tratadas, as taxas de mortalidade podem ser altas nos animais gravemente afetados.
Um eficiente controle dos vermes só é possível através da integração de vários métodos, como manejo de pastoreio, suplementação nutricional, uso estratégico de anti-helmínticos, bem como seleção de animais resistentes, todos contidos em um programa integrado (CSIRO, 2007). Entretanto, a forma de combate mais utilizada pelos criadores é o tratamento farmacológico, mas o uso indiscriminado fez surgir um fenômeno denominado de resistência anti-helmíntica. Esta é responsável pela perda da eficácia dos princípios ativos mais utilizados, em virtude do surgimento de vermes que não são afetados por eles. Além disso, a crescente demanda por produtos orgânicos em todo o mundo encorajou uma busca por métodos alternativos para controlar a helmintíase em ovinos (Benavides et al., 2015)
A seleção de animais capazes de resistir às infecções por parasitas gastrintestinais e a sua utilização em sistemas de acasalamento surge como uma opção de controle às parasitoses, diminuindo a necessidade de uso constante de drogas.
Seleção de animais resistentes
Ovinos mostram considerável variação genética em sua capacidade de limitar e resistir a infecções por vermes (Arsenopoulos et al., 2017). A capacidade de selecionar animais para melhorar a resistência a nematóides é dependente desta variação e da capacidade do criador identificar e utilizar animais resistentes nos processos de acasalamento (Bishop, 2012).
Um animal considerado resistente é aquele que possui maior capacidade de prevenir o estabelecimento de larvas de parasitas e promover a eliminação de qualquer uma que se estabeleça (Bishop, 2012). Essa resistência à parasitose é uma variável de mensuração indireta, onde geralmente são avaliadas características como a contagem de ovos por grama de fezes (OPG), variáveis hematológicas como o volume globular (Hematócrito), bem como o escore Famacha®. Essas caraterísticas geralmente possuem herdabilidade variando entre 0,2-0,7 (Zvinorova et al., 2016).
Um dos principais fenótipos mensurados e considerado padrão na busca por animais resistentes é a contagem de ovos por grama de fezes (OPG). Esta característica está relacionada com a carga parasitária e com o grau de contaminação das pastagens (Lôbo et al., 2009), pois o animal mais resistente excretará menos ovos. Portanto, quanto menor for o OPG menos susceptível é o animal à verminose, além de contribuir menos com a contaminação dos pastos. Aliado a isso, este indicador é eficiente para vários gêneros de nematódeos, devido à forte correlação genética existente entre os valores de OPG e a contagem das diferentes espécies de nematoides. Logo, a seleção com base nos valores genéticos para OPG tende a aumentar a resistência a diferentes espécies de parasitos.
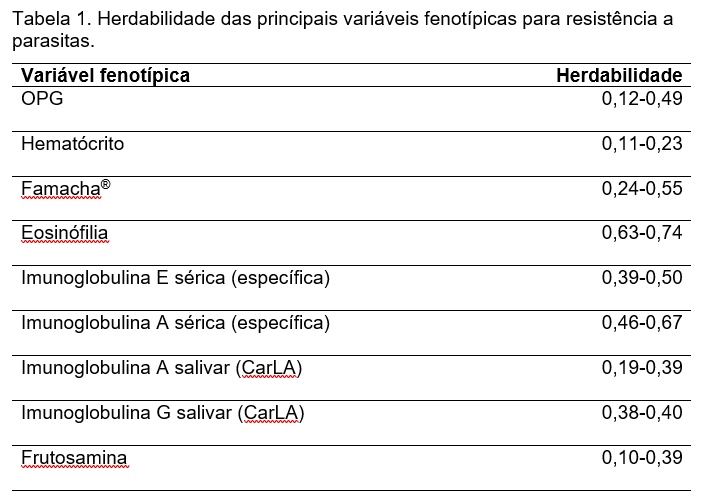
Diversos estudos têm demonstrado herdabilidade moderada para OPG (Tabela 1). Segundo Bishop (2012), este parâmetro genético varia entre 0,2 a 0,4 e Lôbo et al. (2009) estimaram herdabilidade de até 0,52 em cordeiros da raça Santa Inês. A herdabilidade de uma característica indica se existe a possibilidade de obter ganho genético quando a mesma é usada em processos de seleção e esses valores citados sugerem que a seleção para resistência por meio da variável OPG é viável a médio e longo prazos (McRae et al., 2014). Exemplos bem-sucedidos foram demonstrados em experimentos na Nova Zelândia e na Austrália (CSIRO, 2007).
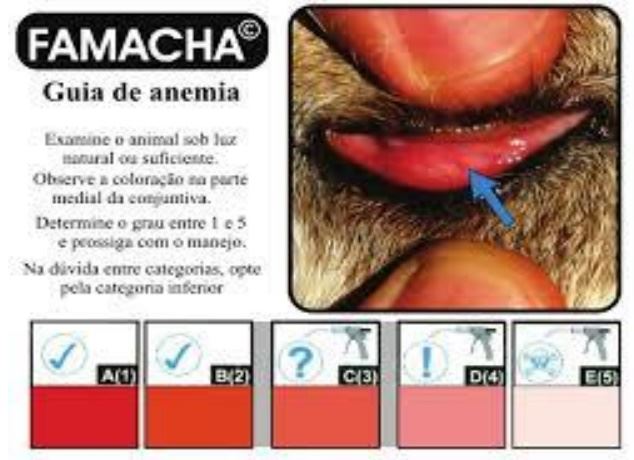
Haemonchus contortus é o parasita economicamente mais importante para a produção de pequenos ruminantes em muitas regiões do mundo, inclusive no Brasil. Trata-se de um parasito hematófago e, portanto, importante causador de anemia. O método Famacha® (figura 1), desenvolvido na África do Sul, é utilizado para identificar animais anêmicos, os quais podem estar infectados por este verme. Nestes métodos são categorizados cinco graus de coloração da mucosa ocular, onde o nível 1 é a mucosa vermelha e o nível 5 a coloração mais pálida. De acordo com Riley e Van Wyk (2009), este indicador possui herdabilidade entre 0,24 e 0,55, enquanto Ngere et al. (2017) observaram herdabilidade variando de 0,32 a 0,41. Desta maneira, é possível adotar critérios de seleção para ovelhas com base nas diferenças entre o histórico de pontuação individual do Famacha®.
O Famacha é um método bastante prático para identificar animais anêmicos e pode ser realizado dentro de um aprisco, mas requer treinamento e pode ser bastante subjetivo. Assim, em um ambiente laboratorial pode se ter um método mais objetivo, que é a mensuração do volume globular ou hematócrito, um exame relativamente barato, cuja única especificidade é a técnica para coleta de sangue dos animais. Este é um bom indicador de como o animal está conseguindo lidar com os efeitos patogênicos da parasitose, principalmente pelo H. contortus. Nos ovinos, essa característica apresenta herdabilidade variando entre 0,18 a 0,22 (Ngere et al., 2017), além de possuir correlação genética negativa com OPG. Portanto, um programa de seleção que visa aumentar a tolerância a parasitos gastrointestinais busca sempre diminuir a contagem de ovos por grama de fezes e o escore Famacha®, ou aumentar o volume globular (Bishop, 2012).
Outras variáveis, de caráter imunológico, também podem ser utilizadas em estudos relacionados à resistência aos parasitas gastrintestinais. Entre elas estão contagem de eosinófilos sanguíneos, identificação anticorpos específicos como as imunoglobulinas IgA, IgG, IgM e IgE, anticorpo específico para larvas dosado na saliva (CarLA) e frutosaminas (Bishop, 2012). Todas essas medidas mostram propriedades desejáveis para um processo de seleção, como moderada a alta herdabilidade (Tabela 1), o que indica que a variação genética é um dos componentes mais importantes na variabilidade da atividade imune entre os animais. Amarante et al. (2009) observaram correlação negativa entre IgG específica para H. contortus e contagem de eosinófilos com a contagem de ovos nas fezes (-0,78 e -0,64 respectivamente). Além disso, Murphy et al. (2010) encontraram correlação de -0,2 entre IgE específica para Teladorsagia circumcincta e OPG. Logo, animais que produziram mais anticorpos apresentaram menor OPG e, portanto, foram mais resistentes.
CarLA: antígeno carboidrato larval de superfície
Fonte: Adaptado de Davies et al. (2005) e Zvinorova et al. (2016)
Os traços de caráter imunológico citados acima, podem ser de interpretação complicada por fazerem parte de uma resposta dinâmica do animal frente ao desafio parasitário, mudando com o tempo e sendo afetadas por exposições anteriores aos nematoides. Além disso, possuem custo de avaliação geralmente mais alto, o que dificulta sua aplicação em grande escala. Consequentemente, programas de melhoramento geralmente focam principalmente no OPG, hematócrito e Famacha® (Bishop, 2012).
Conclusão
As principais características fenotípicas relacionadas à resistência aos parasitas gastrintestinais estão sujeitas a variações genéticas e possuem herdabilidade moderadas, podendo ser utilizadas para atingir ganho genético. Desta forma tais variáveis podem ser combinadas com informações de pedigree para estimar valores genéticos dos animais, auxiliando na seleção dos animais mais tolerantes as parasitoses.
Referências bibliográficas
AMARANTE A.F.T., SUSIN I., ROCHA R.A., SILVA M.B., MENDES C.Q., PIRES A.V. 2009. Resistance of Santa Ines and crossbred ewes to naturally acquired gastrointestinal nematode infections. Veterinary Parasitology 165, 273–280.
ARSENOPOULOS K., SYMEONIDOU I., PAPADOPOULOS E. 2018. Immune and other factors modulating host resistance against gastrointestinal nematode parasites in sheep. Journal of the Hellenic Veterinary Medical Society, 68(2), 131-144.
BENAVIDES M.V., SONSTEGARD T.S., KEMP S., MUGAMBI J.M., GIBSON J.P., BAKER R.L., HANOTTE O., MARSHALL K., TASSELL C.V. 2015. Identification of Novel Loci Associated with Gastrointestinal Parasite Resistance in a Red Maasai x Dorper Backcross Population. PLoS ONE 10(4), e0122797.
BISHOP S.C. 2012. Possibilities to breed for resistance to nematode parasite infections in small ruminants in tropical production systems. Animal 6(5), 741–747.
CENCI, F.B., LOUVANDINI, H., MCMANUS, C., DELL’PORTO, A., COSTA, D.M., ARAUJO, S.C., MINHO, A.P., ABDALLA, A.L. 2007. Effects of condensed tannin from Acacia mearnsii on sheep infected naturally with gastrointestinal helminthes. Veterinary Parasitology 144, 132–137.
CSIRO. Breeding sheep for sustainable worm control information sheet, http://www.csiro.au/resources/pfb8.html.
DAVIES G., STEAR M.J., BISHOP S.C. 2005. Genetic relationships between indicator traits and nematode parasite infection levels in 6-month-old lambs. Animal Science 80, 143-150.
LÔBO R.N., VIEIRA L.S., OLIVEIRA A.A.D., MUNIZ E.N., SILVA J.M.D. 2009. Genetic parameters for faecal egg count, packed-cell volume and body-weight in Santa Inês lambs. Genetic Molecular Biology 32, 228-294.
MCRAE K.M., MCEWAN J.C., DODDS K.G., GEMMELL N.J. 2014. Signatures of selection in sheep bred for resistance or susceptibility to gastrointestinal nematodes. BMC Genomics 15, 637.
MURPHY L, ECKERSALL P.D., BISHOP S.C., PETTIT J.J., HUNTLEY J.F., BURCHMORE R., STEAR M.J., 2010. Genetic variation among lambs in peripheral IgE activity against the larval stages of Teladorsagia circumcincta. Parasitology 137, 1249–1260.
NGERE L., BURKEB J.M., HERRINGA A.D., SANDERSA J.O., CRAIGD T.M., VAN WYKE J.A., RILEYA D.G. 2017. Utilization of year-round data in the estimation of genetic parameters for internal parasite resistance traits in Dorper sheep. Small Ruminant Research 151, 5–10.
RILEY D.G., VAN WYK J.A. 2009. Genetic parameters for FAMACHA score and related traits for host resistance/resilience and production at differing severities of worm challenge in a Merino flock in South Africa. Veterinary Parasitology 164, 44–52.
ZVINOROVA P.I., HALIMANI T.E., MUCHADEYI F.C., MATIKA O., RIGGIO V., DZAMA K. 2016. Breeding for resistance to gastrointestinal nematodes − the potential in low-input/output small ruminant production systems. Veterinary Parasitology 225,19-28.