As bactérias ácido-lácticas (BALs) são micro-organismos presentes em leite e derivados e representam a microbiota dominante do intestino de humanos e de animais (JENSEN et al., 2012; KASSAA et al., 2014). São largamente utilizadas em processos industriais, especialmente na fabricação de derivados lácteos, como queijos, iogurtes e bebidas lácteas. Realizam o processo de fermentação através da conversão de carboidratos em, principalmente, ácido láctico, diminuindo o pH do meio e contribuindo com as características sensoriais dos alimentos fermentados, como sabor, aroma e textura (IKEDA et al., 2013; BRUNO; CARVALHO, 2009).
O microencapsulamento de micro-organismos é uma técnica de empacotamento, que visa proteger e preservar as células de condições adversas, tais como, elevadas concentrações salinas e temperaturas, e pHs extremamente ácidos, mantendo o micro-organismo viável por um maior período de tempo. As cápsulas seladas liberam seu conteúdo gradativamente, sob influência das condições que são expostas (ANAL; STEVENS, 2005; ANAL; SINGH, 2007). No entanto, para que o microencapsulado seja viável industrialmente, deve manter a sua capacidade de acidificação, produzindo ácido láctico e liberando-o por difusão, propriedade que depende diretamente do material de parede utilizado (SILVA et al., 2014; VIVEK, 2013).
O soro de queijo e o permeado de soro, subprodutos lácticos, possuem propriedades para serem empregados como constituintes do agente encapsulante. Juntamente com o material gelificante, podem formar uma cápsula externa fina, rígida e semipermeável, ideal para o encapsulamento de bactérias (AZEREDO, 2005; DE OLIVEIRA; BRAVO; TONIAL, 2012).
Dessa forma, o objetivo desse trabalho foi avaliar a capacidade de acidificação no leite de bactérias ácido-lácticas microencapsuladas com material de parede composto por soro de queijo ou permeado de soro.
Metodologia
Os micro-organismos microencapsulados foram o Lactobacillus plantarum ATCC 8014, e dois isolados de leite in natura proveniente do Vale do Taquari/RS, o Lactobacillus paracasei ML 33 e o Lactobacillus pentosus ML 82.
As BALs foram inoculadas em 15 mL de caldo de Man Rogosa and Sharpe (MRS) e mantidas em estufa a 32 ºC por 48 horas. A contagem celular foi padronizada em 109 UFC.mL-1 e o cultivo foi centrifugado a 2370 x g, 4 ºC por 10 minutos, e lavado duas vezes com Phosphate Buffered Saline (PBS), nas mesmas condições anteriores. Posteriormente, as células microbianas foram transferidas para a mistura de 1:1:1 de alginato, pectina e soro de queijo ou permeado de soro, material de parede empregado no microencapsulamento das BALs.
A mistura foi acoplada com uma seringa injetora ao Encapsulator (B-395® BUCHI) numa vazão de 5 mL.min-1, com bico de 80 µm em constante vibração numa frequência de 1740 Hz e eletrodo de 950 mV. Após o processo de formação das microcápsulas, elas foram polimerizadas na solução de CaCl2 0,5 M por 30 minutos sob agitação magnética, filtradas e ressuspendidas em 100 mL de leite, que foi mantido em estufa a 37 ºC. O pH do leite foi determinado periodicamente, até atingir valor de 4,6. Além disso, também foi determinada a capacidade de acidificação das BALs não encapsuladas.
Resultados e discussão
A Tabela 1 apresenta os resultados de acidificação do leite das BALs microencapsuladas, com soro de queijo ou permeado de soro, e não microencapsuladas (célula livre).
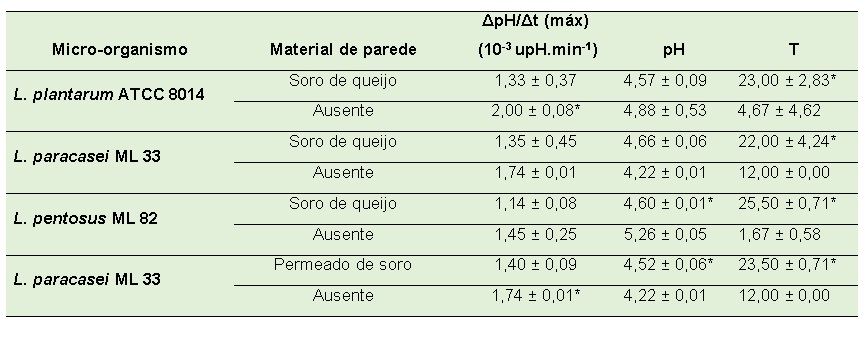
Tabela 1. Avaliação do potencial de acidificação do leite a 37 ºC dos micro-organismos microencapsulados ou não.
ΔpH/Δt (máx): taxa máxima de acidificação, calculada pela variação do pH sobre a variação do tempo em minutos. pH: valor de pH correspondente à taxa máxima de acidificação. T: tempo em horas para atingir a taxa máxima de acidificação.*Resultados na mesma coluna para cada microrganismo apresentam diferença significativa (P<0,05), n=3.
O L. plantarum ATCC 8014 microencapsulado com soro e o L. paracasei ML 33 microencapsulado com permeado apresentaram, em relação às respectivas células livres, diferença estatística (P<0,05) na taxa máxima de acidificação. A menor capacidade de acidificação dos micro-organismos microencapsulados é devido à proteção que o material de parede possibilita, retardando o processo de acidificação no leite.
Em relação ao tempo em horas para atingir a taxa máxima de acidificação, é possível constatar que todos os micro-organismos microencapsulados quando comparados à célula livre apresentaram diferença estatística (P<0,05), apresentando valores elevados, indicando que o processo de acidificação do leite foi retardado devido ao processo de difusão que ocorre em presença da cápsula protetora.
Nesse contexto, pode-se afirmar que a célula se mantém viável quando microencapsulada com soro de queijo e permeado de soro, uma vez que apresenta capacidade de acidificação, porém de forma mais lenta quando comparada à célula livre, e pode ser empregada na elaboração de produtos fermentados.
Referências bibliográficas
ANAL, A. K.; STEVENS, W. F. Chitosan-alginate multilayer beads for controlled release of ampicillin. International Journal of Pharmaceutics, v. 290, p. 45-54, 2005.
ANAL, A. K.; SINGH, H. Recent advances in microencapsulation of probiotics for industrial applications and targeted delivery. Trends in Foods Science & Technology, v.18, p. 240-251, 2007.
AZEREDO, H. M. C. Encapsulação: aplicação à tecnologia de alimentos. Alimentos e Nutrição, v. 16, p. 89-97, 2005.
BRUNO, L. M.; CARVALHO, J. D. G. Microbiota lática de queijos artesanais. Embrapa Agroindústria Tropical. Documentos. 2009.
DE OLIVEIRA, F.; BRAVO, C. E. C; TONIAL, I. B. Soro de leite: um subproduto valioso. Revista do Instituto de Laticínios Cândido Tostes, v. 67, n. 385, p. 64-71, 2012.
IKEDA, D. M.; WEINERT JR., E.; CHANG, K. C. S.; MCGINN, J. M.; MILLER, S. A.; KELIIHOOMALU, C.; DUPONTE, M. W. Natural farming: Lactic acid bacteria. University of Hawai. College of Tropical Agriculture and Human Resource. Sustainable Agriculture, 2013.
JENSEN, H.; GRIMMER, S.; NATERSTAD, K.; AXELSSON, L. In vitro testing of commercial and potential probiotic lactic acid bacteria. International Journal of Food Microbiology, v. 153, p. 216–222, 2012.
KASSAA, I. A.; HOBER, D.; HAMZE, M.; CHIHIB, N. E.; DRIDER, D. Antiviral potential of lactic acid bacteria and their bacteriocins. Probiotics and Antimicrobial Proteins, v. 6, p. 177–185, 2014.
SILVA, P. T. D.; FRIES, L. L. M.; MENEZES, C. R. D.; HOLKEM, A. T.; SCHWAN, C. L.; WIGMANN, E. F.; SILVA, C. D. B. D. Microencapsulation: concepts, mechanisms, methods and some applications in food technology. Ciência Rural, v. 44, p.1304-1311, 2014.
VIVEK, K. Use of encapsulated probiotics in dairy based foods. International Journal of Food, Agriculture and Veterinary Sciences, v. 3, p. 188-99, 2013.
Dados inválidos!
Verifique suas credenciais e tente novamente: atente-se aos caracteres em
maiúsculo e minúsculo.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
Acesso a matérias, novidades por newsletter, interação com as notícias e muito mais.
ENTRAR SOU UM NOVO USUÁRIO