A refrigeração do leite na propriedade e o transporte a granel foram implementados com o objetivo de melhorar a qualidade do leite cru e consequentemente dos seus derivados. Com esta mudança, acreditou-se aumentar o tempo da vida de prateleira de queijos, iogurtes, leites fermentados, leite UHT e demais produtos lácteos, além da melhoria sensorial. Porém, a baixa qualidade microbiológica da matéria-prima que é armazenada sob refrigeração contribuiu para aumentar a contagem de micro-organismos psicrotróficos.
Sabe-se que a partir de uma população, que varia na literatura entre 105 e 107 UFC/mL, os psicrotróficos produzem enzimas extracelulares termorresistentes que promovem alterações nos derivados lácteos como rancidez, sabor amargo, geleificação em leite UHT, redução da capacidade térmica do leite em pó e aumento da capacidade de formar espuma em leite reconstituído. Ainda pode-se ter resultado falso-positivo na pesquisa por fraude de leite com soro por meio da dosagem do ácido siálico e redução no rendimento na fabricação de queijos.
As enzimas bacterianas podem ser proteases, lipases e fosfolipases (lecitinase) e sua síntese está relacionada à temperatura de estocagem do alimento, fase de crescimento do micro-organismo, disponibilidade de oxigênio e composição do meio. Sua atividade é dependente de temperatura, pH e concentração do substrato.
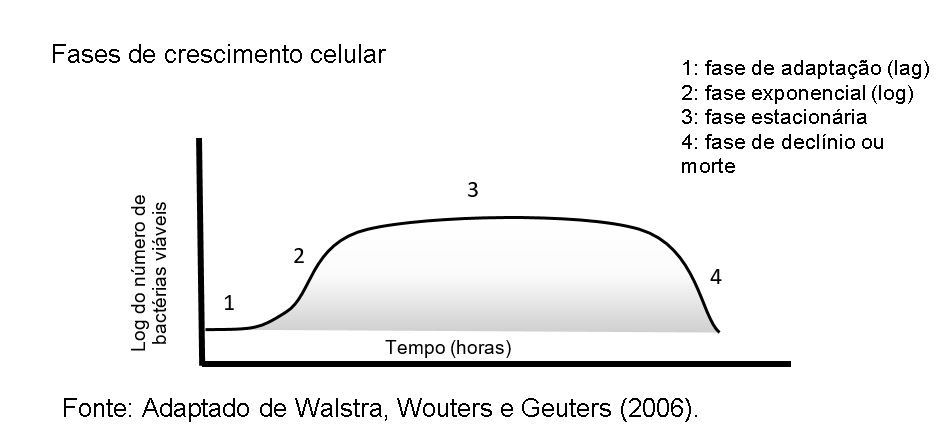
É importante lembrar que a atividade e a frequência enzimática podem variar com o tipo de micro-organismo psicrotrófico presente no leite. A produção enzimática por Pseudomonas spp., por exemplo, ocorre sob refrigeração principalmente no final da fase log de crescimento celular e na fase estacionária, sendo a sua síntese maior abaixo da temperatura ótima (20 a 30ºC) de crescimento do micro-organismo.
Proteases, lipases e fosfolipase
A proteólise em leite pode ser causada por proteases naturais chamada plasmina ou por enzimas produzidas por micro-organismos psicrotróficos. A plasmina, derivada do plasminogênio, tem o aminoácido serina como sítio ativo e hidrolisa β-, αS1- e αS2-caseína. Assim, qualquer fator que converta plasminogênio a plasmina pode ter um impacto negativo sobre a proteína do leite. Altas contagens de células somáticas no leite por exemplo, é um fator que contribui para o aumento de plasmina no leite.
Já as proteases produzidas pelos psicrotróficos são geralmente metaloproteinases, isto é, precisam de um íon como o cálcio para atingir sua atividade ótima. Sua atividade é similar à da quimosina, empregada na coagulação do leite e que atua na κ-caseína, provocando a desestabilização das micelas de caseína. As proteases bacterianas estão relacionadas principalmente a processos de geleificação do leite UHT, mas podem ser associadas também a alterações na coagulação e sabor amargo dos queijos.
A lipase é uma glicoproteína e sua ação resulta na hidrólise enzimática dos lipídeos do leite, compostos em média por 98% de triglicerídeos. As lipases podem ser de origem endógena, que em sua maioria estão associadas às micelas de caseína e são termosensíveis a pasteurização, ou de origem exógena, termorresistentes e produzidas por bactérias psicrotróficas.
As lipases naturais podem causar lipólise espontânea e induzida. A primeira confere ao leite recém ordenhado aspecto rançoso e pode estar relacionada ao estágio de lactação (final), nutrição inadequada e aumento do número de ordenhas. Estas condições promovem o aumento de lipoproteína proveniente do sangue para o leite, favorecendo a ação das lipases endógenas. Na lipólise induzida ocorrem danos à membrana do glóbulo de gordura por meios físicos como a agitação, formação de espuma ou homogeneização. Estes processos favorecem a deterioração de produtos sem tratamento térmico pois permitem a ação da lipase endógena, principalmente da lipoprotéica (LLP), promovendo a hidrólise dos triglicerídeos.
Embora as enzimas naturais do leite possam afetar sua vida de prateleira e de seus derivados, as lipases oriundas de micro-organismos psicrotróficos são mais prejudiciais. Pode-se ter defeitos como sabor e odor de ranço e sabão, devido a hidrólise de ácidos graxos, e sabor metálico ou oxidado devido à ação de ácidos graxos insaturados oxidados sobre cetonas e aldeídos.
A lecitinase ou fosfolipase C é um tipo específico de lipase sintetizada por micro-organismos psicrotróficos, capaz de hidrolisar a membrana dos glóbulos de gordura do leite. O resultado são defeitos de sabor e textura conhecidos como leite/creme gorduroso. Além disso, a atividade da fosfolipase favorece a ação das outras lipases.
Dados inválidos!
Verifique suas credenciais e tente novamente: atente-se aos caracteres em
maiúsculo e minúsculo.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
Acesso a matérias, novidades por newsletter, interação com as notícias e muito mais.
ENTRAR SOU UM NOVO USUÁRIO