As gorduras, ou lipídios, são moléculas que influenciam profundamente nas características dos alimentos, tanto na textura quanto no sabor. Modificações químicas nesse componente podem ser desejadas ou não, mas invariavelmente alteram a qualidade do alimento, especialmente nos que têm alto teor de gordura, como queijos e manteiga.
A rancidez em leite e derivados é um processo normalmente associado à deterioração do produto devido ao off-flavour gerado pelos compostos formados nas reações com os lipídios, porém em alguns queijos esse processo pode ser desejável. A rancidez é dividida em hidrolítica e oxidativa, com base no mecanismo químico ou bioquímico que a determina.
Para explorarmos melhor o assunto, é necessário primeiro apresentar alguns pontos relativos à composição do leite, em especial aos lipídios, que é o grupo de moléculas susceptível ao ranço.
Os lipídios no leite
O leite é um fluido bastante complexo, no qual os constituintes estão presentes em três fases — solução, dispersão e emulsão. Os lipídios estão em emulsão no leite, como glóbulos em tamanhos que variam entre 0,1 e 20 μm (FOX et al., 2015). Os glóbulos de gordura são compostos principalmente por triacilgliceróis em seu interior, envolvidos por uma membrana lipoproteica (WALSTRA et al., 2006).
O leite de todas as espécies de mamíferos contém lipídios e a quantidade varia muito entre as espécies (FOX et al., 2015). Pela Instrução Normativa nº 76/2018 do Ministério da Agricultura, Pecuária e Abastecimento, o leite bovino deve apresentar no mínimo 3% (m/m) de gordura (BRASIL, 2018).
No entanto, o teor de gordura é um dos componentes que mais sofre variação no leite, devido a diversos fatores como alimentação e individualidade do animal, estações do ano, estágio de lactação, intervalo entre ordenhas e processamento (FUQUAY et al., 2011). Dessa forma, o teor de gordura no leite bovino pode variar de cerca de 3,0 a 6,0%, mas normalmente está na faixa de 3,5 a 4,7% (McGIBBON; TAYLOR, 2006).
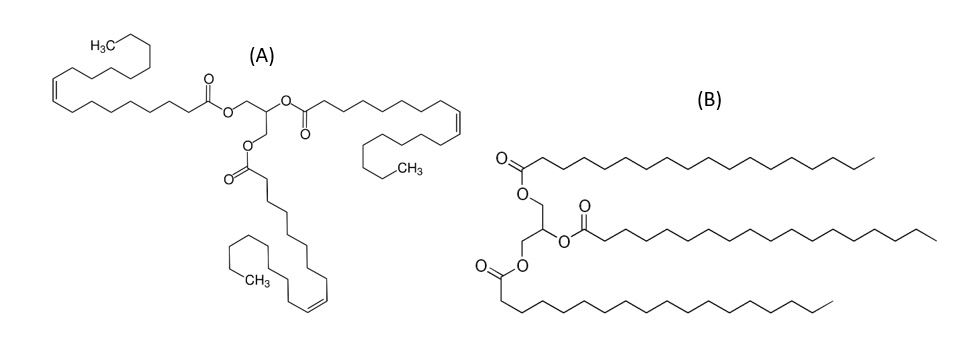
No leite bovino os triacilgliceróis compõem 98% do total de lipídios, contendo ainda diacilgliceróis, monoacilgliceróis, fosfolipídios, ácidos graxos livres, cerebrosídeos, gangliosídeos, colesterol e vitaminas lipossolúveis (SALDANHA et al., 2016). Os triacilgliceróis são moléculas formadas pelo glicerol e três ácidos graxos, como a trioleína e a triestearina, na Figura 1.
Figura 1. Exemplos de triacilglicerol: a trioleína (A) e a triestearina (B).
Fontes: Wikipedia (A); Wikipedia (B)
A composição de ácidos graxos nos triacilgliceróis é bastante variável no leite, pois sofre influência de fatores como alimentação do gado, estágio de lactação, fatores ambientais e climáticos (SALDANHA et al., 2016), como mencionado anteriormente. Os ácidos graxos podem variar no tamanho da cadeia carbônica e no número, posição e configuração de duplas ligações.
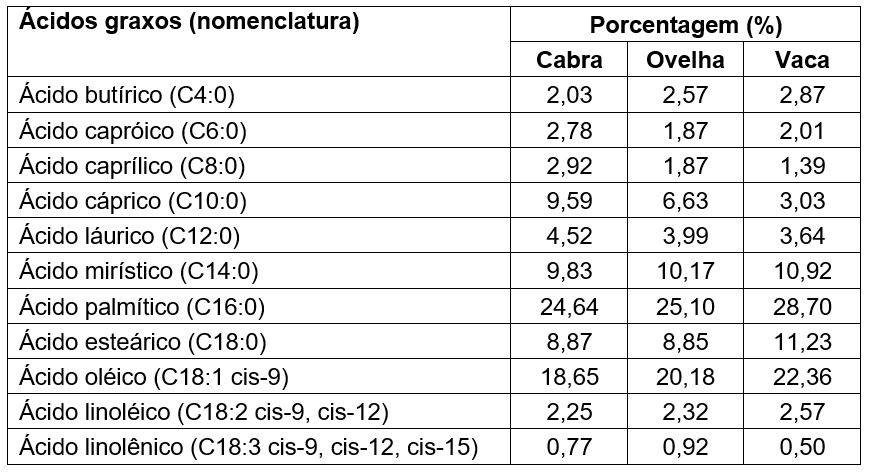
O padrão de ácidos graxos é um fator importante na determinação das propriedades lipídicas, como intervalo de fusão, reatividade química (inclusive susceptibilidade ao ranço) e valor nutricional (WALSTRA et al., 2006). A Tabela 1 mostra o perfil de ácidos graxos no leite de cabra, ovelha e vaca.
Tabela 1. Perfil de ácidos graxos em cabra, ovelha e vaca (percentual em relação ao teor total de ácidos graxos presente no leite de cada espécie).
Fonte: adaptado de MARKIEWICZ-KESZYCKA et al. (2013).
Rancidez hidrolítica
A rancidez hidrolítica está associada com a reação de lipólise, o qual é o processo de hidrólise (“quebra”) dos triacilgliceróis que compõem a gordura. Esta hidrólise ocorre na ligação éster entre ácidos graxos e glicerol por lipases ou pela combinação de calor e umidade, que tem como resultado a liberação de ácidos graxos.
A lipólise ocorre normalmente durante o armazenamento do produto devido à ação de lipases que podem estar naturalmente presentes no alimento, como é no caso do leite, ou devido à contaminação microbiana (ARAÚJO, 2019).
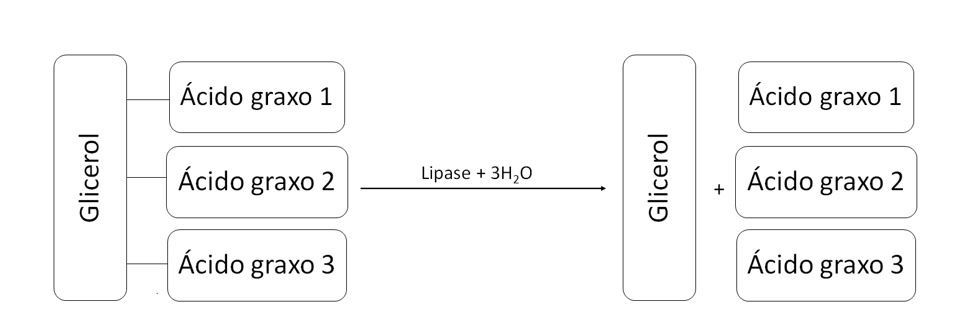
Figura 2. Representação da ação da lipase sobre o triacilglicerol.
Fonte: elaborado pelos autores.
A lipase (E.C. 3.1.1.34) é uma lipoproteína que apresenta temperatura ótima de atuação a 37°C e pH ótimo aproximadamente 9,0. É intensamente inibida por seus produtos, em especial os ácidos graxos de cadeia longa, possivelmente porque se une fortemente a eles. É estimulada por cátions bivalentes como cálcio (Ca2+) presente no leite (FOX et al., 2015).
Fatores atuam conjuntamente sobre a ação enzimática, impedindo a rancidez hidrolítica no leite (WASLTRA; JENNESS, 1984):
- O pH natural do leite e sua composição iônica estão abaixo do considerado ótimo para ação da lipase, diminuindo consideravelmente sua atividade;
- A lipase no leite está em grande parte unida às micelas de caseína, o que diminui muito a concentração de enzima livre e, consequentemente, a sua atividade;
- Além das micelas de caseína, outros inibidores são encontrados no leite em quantidades variáveis, como a proteose peptona 3 (PP3);
- A membrana natural do glóbulo de gordura protege eficazmente os triacilgliceróis do ataque enzimático;
- O leite contém possivelmente quantidades variáveis de estimulantes conhecidos (como o cofator apoproteico) e desconhecidos. Existe assim um sutil equilíbrio entre inibidores e estimulantes da ação da lipase;
- A enzima é instável e no leite perde lentamente a sua atividade potencial. A instabilidade aumenta com a temperatura e com a diminuição do pH. Provavelmente a enzima é mais estável quando está ligada às micelas de caseína;
- A lipase é inativada por aquecimento a 75°C por 20 segundos e em pH 4,6 em 1 hora.
A lipólise da gordura láctea aumenta a concentração de ácidos graxos livres (AGL), o que confere aos produtos um sabor rançoso ou de sabão. A intensidade da lipólise pode ser expressa como índice de acidez da gordura em mmol de AGL por 100 g de gordura. O teor de AGL no leite recém ordenhado é aproximadamente 0,4 g por 100 g de gordura ou 0,15 mmol/L de leite.
No leite fresco varia entre 0,2 a 1 mmol/100g (WASLTRA; JENNESS, 1984). Os índices superiores a 1 mmol AGL/100 g de gordura são indesejáveis para o leite; a partir deste ponto a rancidez já é perceptível sensorialmente em produtos derivados com maior teor de gordura, como o creme (WALSTRA et al., 2006).
Os ácidos graxos de 4 a 10 átomos de carbono conferem ao produto um off-flavour típico. O limiar de percepção do ácido butírico (C4:0) é de 0,5 a 10 ppm e dos ácidos capróico (6:0) e caprílico (8:0) é de 3 ppm (ARAÚJO, 2019). Quanto menor o peso molecular do ácido graxo, ou seja, quanto menor o número de carbonos do ácido graxo maior sua solubilidade em água e maior a sua percepção sensorial. A lipólise pode ocorrer de três formas: induzida, espontânea e microbiana.
Lipólise induzida
A lipólise induzida ocorre quando há deterioração da membrana do glóbulo de gordura (CIMIANO; ALVAREZ, 1983). A ativação do substrato pode ocorrer de três formas: por homogeneização, por formação de espuma e manipulando a temperatura.
Os dois primeiros métodos são muitos semelhantes e se baseiam no fato de que a superfície do glóbulo de gordura nessas condições se recobre de proteínas do plasma e de outras substâncias e esta nova membrana nunca protege a gordura tão bem como fazem as membranas naturais.
Já a manipulação da temperatura (variações entre temperaturas baixas e altas) pode levar à cristalização e modificações na membrana do glóbulo de gordura, favorecendo a lipólise (FUQUAY et al., 2011).
Os problemas originados pela lipólise (como sabor rançoso) são a princípio uma combinação de fatores: a agitação demasiada e intensa do leite, especialmente quando se bate o ar incorporado; quando uma grande proporção do leite é proveniente de animais nos últimos estágios de lactação, padecem de mastite ou estão deficientemente alimentados (WASLTRA; JENNESS, 1984).
O dano à membrana pode ocorrer em diversos estágios do processo de ordenha: formação de espuma devido ao ar adicionado, agitação devido às seções verticais das tubulações, constrições ou expansões nas tubulações, bombas e especialmente se não está operando em capacidade máxima, superfícies de resfriadores, agitadores nos tanques e congelamento de leite nas paredes dos resfriadores.
A frequência e severidade da lipólise aumenta com o final da lactação, possivelmente devido à fragilidade da membrana do glóbulo de gordura e ao baixo nível de leite produzido, o que pode agravar a agitação; esse problema é particularmente agudo quando o leite produzido é sazonal (FOX; McSWEENEY, 2006).
Lipólise espontânea
A lipólise, e consequentemente a rancidez hidrolítica, podem ocorrer de forma espontânea no leite. Os mecanismos de lipólise espontânea estão geralmente ligados ao animal: indivíduo, período de lactação e alimentação (CIMIANO; ALVAREZ, 1983).
Normalmente o leite não se rancifica espontaneamente, embora o leite de algumas vacas possa se mostrar sensível à lipólise. A variação de sensibilidade à lipólise entre leites de vacas individuais possivelmente se deve a diferenças nas quantidades de ativadores (ou estimulantes) e inibidores da ação enzimática.
A mastite e estágio avançado de lactação podem aumentar a predisposição da gordura à lipólise, aumentando a probabilidade de ocorrência de lipólise espontânea; isso se dá provavelmente por haver mais cofatores que se transferem do sangue para o leite nestas condições.
Há também uma correlação muito alta entre a ocorrência de lipólise espontânea e a quantidade de leite produzido; quando está abaixo de 3 kg por ordenha a probabilidade de lipólise é aumenta. A alimentação animal com ração de baixa qualidade também faz com que a probabilidade de lipólise aumente (WASLTRA et al., 2006; FOX et al., 2015).
Lipólise microbiana
A lipólise microbiana ocorre em leite armazenado em baixas temperaturas com o desenvolvimento de bactérias psicrotróficas que produzem lipases (BONASSI, 1989). Neste caso o leite poderá conter lipases bacterianas termoestáveis que podem inclusive resistir parcialmente ao tratamento UHT e quando o leite se conserva por muito tempo armazenado, uma pequena quantidade de lipase residual pode causar rancificação (WASLTRA et al., 2006). Lipases de origem bacteriana podem apresentar atividade mesmo em temperaturas muito baixas; 50% da atividade dessas enzimas ainda pode ser observada a 0°C (CIMIANO; ALVAREZ, 1983).
Rancidez Oxidativa
A oxidação é uma das principais causas de deterioração em alimentos, pois altera a qualidade sensorial, valor nutricional, funcionalidade e toxidez do produto. A reação começa nos lipídios e acaba envolvendo outros componentes como proteínas, vitaminas e pigmentos. A rancidez oxidativa se dá pela oxidação de lipídios, que consiste numa série de reações químicas envolvendo ácidos graxos insaturados (os que contém duplas ligações) e oxigênio (ARAÚJO, 2019).
Os lipídios em alimentos podem ser oxidados segundo três mecanismos distintos, a saber: auto-oxidação, foto-oxidação (químicos) e enzimático (por ação da lipoxigenase). O mecanismo enzimático de oxidação de lipídios não é importante em leite e derivados, pois a lipoxigenase não está presente nestes produtos.
Auto-oxidação
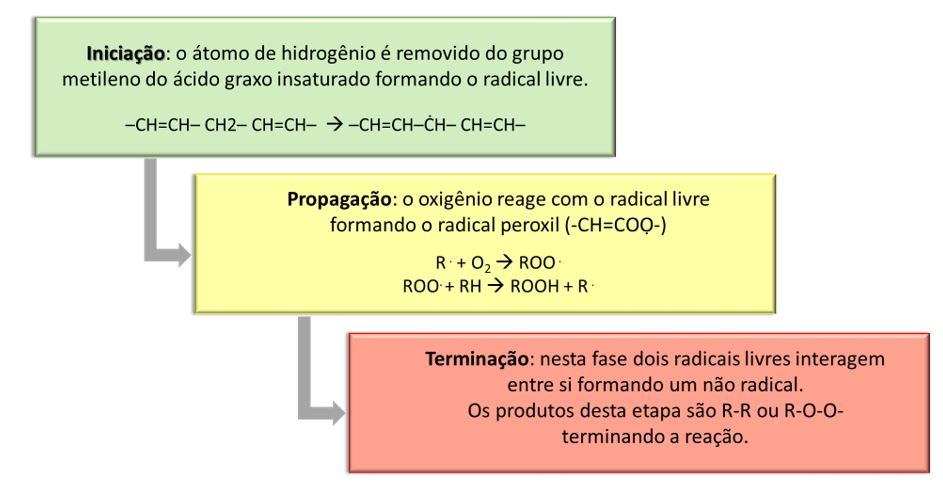
Os ácidos graxos insaturados, tanto livres como ligados aos triacilgliceróis, se oxidam. Este mecanismo acontece por uma série de reações que ocorrem em três etapas: iniciação, propagação e terminação, como esquematizado na Figura 3.
Na iniciação, o primeiro radical livre é formado retirando-se um hidrogênio da cadeia do ácido graxo, em uma posição próxima à dupla ligação. Apesar de ácidos graxos saturados poderem perder um hidrogênio e se submeter à oxidação, a reação envolve principalmente ácidos graxos insaturados, especialmente poli-insaturados, sendo o grupo metileno (–CH2–) entre duplas ligações o mais sensível.
Os lipídios polares na gordura do leite, como os fosfolipídios, são mais ricos em ácidos graxos poli-insaturados (AGPI) que os lipídios neutros (triacilgliceróis) e são concentrados na membrana do glóbulo de gordura em posição próxima com diversos pró-oxidantes e são, assim, particularmente sensíveis à oxidação (DALA-PAULA et al., 2020).
A reação inicial ocorre pela ação de alguma forma externa de energia, como calor, luz, radiação ou por meio de reações químicas envolvendo metais ou metaloproteínas (ARAÚJO, 2019). O conteúdo de cobre presente é importante, pois este metal é um forte catalizador da reação de oxidação, facilitando inclusive que os triacilgliceróis se oxidem (WASLTRA; JENNESS, 1984).
Na propagação, o oxigênio reage com o radical livre formando o radical peroxil (-CH=CO?-), muito reativo e capaz de remover átomos de hidrogênio de outros ácidos graxos insaturados. Estas reações podem ocorrer por si mesmas resultando em hidroperóxidos (DALA-PAULA et al., 2020). Na terminação, a presença de radicais livres já é tão alta que acabam interagindo entre si formando um não radical. Ocorre a polimerização e formação de peróxidos (DALA-PAULA et al., 2020).
Figura 3. Quadro esquemático das etapas da auto-oxidação: iniciação, propagação e terminação.
Fonte: elaborado pelos autores com informações de Araújo (2019).
Foto-oxidação
A presença de fotosensores nos tecidos animal e vegetal, como a riboflavina, clorofila e mioglobina, na presença de luz e oxigênio, dá início ao processo de transferência de energia para o oxigênio, modificando-o de uma forma inerte para uma forma reativa.
Os sensores são capazes de absorver luz na região do visível e/ou perto do ultravioleta (UV) e transferir essa energia para o oxigênio atmosférico, ativando-o e tornando-o capaz de oxidar os ácidos graxos insaturados, formando peróxidos (ARAÚJO, 2019; DALA-PAULA et al., 2020).
Degradação do peróxido
Nos dois mecanismos de oxidação citados (auto-oxidação e foto-oxidação), ocorre a formação de peróxidos. Essas substâncias são instáveis e correntemente se degradam formando numerosos produtos, especialmente cetonas e aldeídos e alguns álcoois e ácidos com aroma pronunciado. Muitos desses compostos são voláteis e contribuem com o flavour de ranço característico.
Os hidroperóxidos, que são os principais produtos da auto-oxidação, não têm aroma, mas podem ser quebrados em diversos produtos, incluindo carbonilas insaturadas, que são as principais responsáveis pelo off-flavour de lipídios oxidados. Diferentes carbonilas variam em função do impacto e tipo do flavour. Os metais como o ferro e o cobre podem participar da degradação de peróxidos resultando na formação de radicais livres.
Os aldeídos formados podem sofrer reações posteriores de condensação, formando outras moléculas, e também podem ser oxidados a ácido carboxílico. Álcool e hidrocarboneto também são formados, dependendo da posição de quebra do peróxido (ARAÚJO, 2019; FOX; McSWEENEY, 2006).
Fatores que influenciam a oxidação de lipídios no leite
Alguns fatores químicos e tecnológicos interferem nas reações oxidativas dos lipídios. Estes fatores atuam não somente no leite, mas também em seus derivados. O processamento pode afetar muito o desenvolvimento de sabores oxidados e para assegurar uma boa qualidade de conservação é importante otimizar as condições de processamento (WASLTRA; JENNESS, 1984).
A estabilidade oxidativa do leite é um resultado de um delicado balanço entre processos pró-oxidantes e antioxidantes, influenciados por fatores como nível de insaturação de ácidos graxos, conteúdo de íons metálicos de transição e de antioxidantes como tocoferóis e carotenóides.
Entretanto, fatores como processamento, embalagem e condições de estocagem também afetam a vida de prateleira do leite pasteurizado e derivados, já que os mecanismos principais de deterioração da qualidade destes produtos são a oxidação química pela entrada de oxigênio e foto-oxidação (SMETA et al., 2008).
Atividade de água (Aw)
Na desidratação de alimentos ocorrem três eventos: as moléculas que compõem o alimento são aproximadas, o que aumenta probabilidade de interação; há formação de microcapilares com a saída de água que facilita entrada de oxigênio atmosférico; aumenta a sensibilidade química dos componentes do alimento devido à remoção de água de hidratação protetora dos sítios reativos das moléculas nos alimentos.
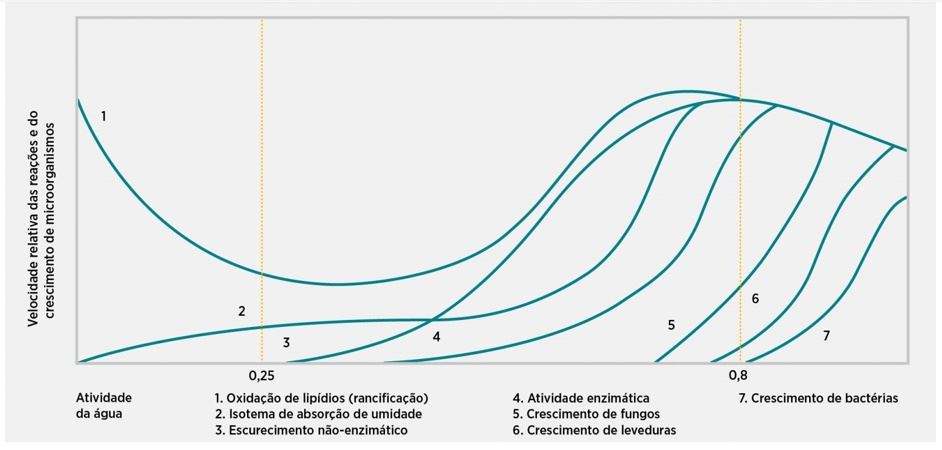
Dessa forma, mínima oxidação ocorre em Aw de aproximadamente 0,3. Porém, em valores menores e maiores que 0,3 a oxidação de lipídios ocorre com maior intensidade, como pode ser observado na Figura 4 (ARAÚJO, 2019).
Figura 4. Velocidade relativa de algumas reações químicas em função da atividade de água (Aw).
Fonte: btaaditivos.
Temperatura
Tratamentos térmicos dão lugar a diversas reações químicas como a reação de Maillard, hidrólises e degradação de proteínas que afetam as propriedades nutricionais e organolépticas do produto. Apesar disso, tem sido demonstrado que o tratamento térmico pode melhorar a capacidade antioxidante do produto.
Esse efeito pode ser atribuído à desnaturação proteica que expõe grupos tiol, que agem como um doador de átomo de hidrogênio e inativam compostos sensíveis à oxidação. A ação antioxidante de alguns produtos da reação de Maillard foram demonstrados (GIROUX et al., 2008).
Acidez/pH
A velocidade da oxidação lipídica é aumentada ao diminuir o pH, sendo o pH ideal da reação de oxidação em aproximadamente 3,8. Já o ranço hidrolítico, que depende da ação da lipase, tem o pH ideal de aproximadamente 9,0 (WASLTRA; JENNESS, 1984).
Homogeneização
A homogeneização reduz acentuadamente a propensão à rancidez oxidativa, tanto se é induzida por cobre ou por luz. Talvez isso ocorra devido à redistribuição de lipídios susceptíveis e pró-oxidantes da membrana do glóbulo de gordura.
Entretanto, a propensão à rancidez hidrolítica e flavour de oxidado pela luz devido à produção de metional de metionina em proteínas é aumentada. Para induzir a auto-oxidação dos glóbulos de gordura recombinados se necessita muito mais cobre (FOX et al., 2015).
Presença de pró-oxidantes
Provavelmente os principais pró-oxidantes em leite e derivados são os metais, cobre e numa extensão menor o ferro, e a luz. Os metais podem estar presentes naturalmente no leite como parte da xantina oxidase, lactoperoxidase, catalase ou citocromos, ou pode surgir por contaminação com aqueles metais oriundos do uso de equipamentos e insumos.
Enzimas que contém metais como lactoperoxidase (contém aproximadamente 0,07% de ferro), catalase (contém ferro) e citocromos podem agir como pró-oxidantes, mais devido ao seu metal que enzimaticamente. Xantina oxidase, que contém ferro e molibdênio, pode agir enzimaticamente como uma fonte de metais pró-oxidantes (FOX et al., 2015).
O citocromo da membrana do glóbulo de gordura pode estar implicado na iniciação da rancidez oxidativa, talvez pela formação de oxigênio singlete – o oxigênio ativado. Riboflavina (vitamina B2) é um potente fotosensor e catalisa um número de reações oxidativas em leite, como em ácidos graxos e proteínas gerando aldeídos que são responsáveis pelo off-flavour induzido pela luz (WASLTRA et al., 2006).
Presença de antioxidantes
Leite e derivados contêm vários antioxidantes, sendo os seguintes provavelmente os mais importantes: tocoferóis (vitamina E), ácido ascórbico (vitamina C - em baixas concentrações como no leite age como um efetivo antioxidante. Porém, age como um pró-oxidante em altas concentrações), os grupos tiol da β-lactoglobulina e proteínas da membrana do glóbulo de gordura que são ativados pelo aquecimento (maiores evidências mostram que os grupos tiol tem propriedades antioxidantes, mas eles podem também produzir espécies de oxigênios ativos, que podem agir como pró-oxidantes em determinadas circunstâncias), caseínas (são efetivos antioxidantes, provavelmente devido a sua ação quelante de cobre), alguns produtos da reação de Maillard (FUQUAY et al., 2011).
O β-caroteno é tido como um dos mais potentes eliminadores de oxigênio singlete; uma molécula é capaz de reagir com 250 a 1000 moléculas de oxigênio singlete. O β-caroteno confere ao leite uma boa proteção contra a oxidação lipídica induzida pela luz e à degradação de riboflavina. A proteção da riboflavina se dá pela competição por absorção de luz pelo caroteno (FOX et al., 2015).
Embalagem
O tipo de embalagem usada em leite e derivados pode afetar substancialmente a qualidade do leite e seus derivados por controlar diretamente a quantidade de oxigênio e de luz disponível para interagir com o produto, bem como por prover perfeita selagem com o objetivo de evitar contaminação pós-pasteurização por microrganismos (VASSILAA et al., 2002).
A embalagem pode diretamente prevenir o desenvolvimento de off-flavour, alteração de textura, redução do valor nutritivo e descolaração induzido pela luz por proteger o produto tanto de oxigênio quanto da luz (MOYSSIADIA et al., 2004).
A Figura 5 mostra o butteroil ou gordura anidra de leite, um produto com 99,7% de gordura produzido a partir do aquecimento da manteiga ou creme de leite, que foi armazenado em embalagem transparente na presença de oxigênio e exposto a luz ou não.
A rancificação oxidativa deste produto com alto teor de gordura quando exposto a luz e oxigênio levou a descoloração e alteração de textura. Embalagens ativas, com a presença de antioxidantes como tocoferóis, ou com baixa permeabilidade ao oxigênio e transmissão de luz, além de uso do vácuo ou gás inerte, são estratégias usadas com o objetivo de diminuir a deterioração por rancificação em alimentos, inclusive lácteos (GIROUX et al., 2008; LEE et al., 2004).
Figura 5. Rancificação oxidativa de butteroil armazenado em embalagem transparente na presença de oxigênio e exposto a luz ou não.
Fonte: elaborado pelos autores.
Considerações finais
A rancificação da gordura láctea é reconhecidamente um dos principais fatores que limitam a vida útil dos produtos derivados do leite que contém gordura, embora seja desejada em alguns tipos de queijos. Fatores que colaboram com as reações lipolíticas e oxidativas estão presentes no leite, bem como existem também moléculas e procedimentos capazes de evitar que o ranço indesejável aconteça.
Para manipular esses fatores é preciso conhecê-los e assim utilizá-los a favor da tecnologia, para que produtos com as características desejadas sejam obtidos. O desconhecimento a respeito das reações que levam à rancificação dos produtos lácteos e, consequentemente, tem levado à diminuição de vida de prateleira dos produtos gordurosos e à disponibilização de produtos com má qualidade no mercado.
Referências
ARAÚJO, J. M. A. Química de Alimentos: teoria e prática. 7 ed. Viçosa: UFV, 2019. 666 p.
BONASSI, I. A. Lipólise em Leite e Derivados. Revista do Instituto de Laticínios Cândido Tostes. v.44. n.261/266. p.42-48. 1989.
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Instrução Normativa nº 76, de 26 de novembro de 2018. Regulamentos técnicos que fixam a identidade e as características de qualidade que devem apresentar o leite cru refrigerado, o leite pasteurizado e o leite pasteurizado tipo A. Diário Oficial da União: seção 1, Brasília, DF, n. 230, p. 9, 30 nov. 2018.
CIMIANO, P. C.; ALVAREZ, J. A. G. A lipólise e sua influência na qualidade do leite. Revista do Instituto de Laticínios Cândido Tostes, v. 38. n. 230. p. 27-33, 1983.
DAPA-PAULA, B. M et al. Química & Bioquímica de Alimentos. 1. ed. Alfenas: UNIFAL, 2020.
FOX, P. F. et al. Dairy Chemistry and Biochemistry. 2. ed. Cham, Suíça: Springer, 2015.
FOX, P. F..; McSWEENEY, P. L. H. (ed.). Advanced Dairy Chemistry. Volume 2 – Lipids. 3. ed. New York: Springer, 2006.
FUQUAY, J. W.; FOX, P. F.; McSWEENEY, P. L. H. Encyclopedia of Dairy Sciences. 2. ed. Londres: Elsevier, 2011.
GIROUX, H. J. et al. Effect of electroreduction and heat treatments on oxidative degradation of a dairy beverage enriched with polyunsaturated fatty acids. Food Research International, v. 41. p. 145-153. 2008. DOI: 10.1016/j.foodres.2007.10.008
HAVEMOSEA, M. S. et al. Influence of feeding different types of roughage on the oxidative stability of milk. International Dairy Journal, v. 14, p. 563-570, 2004. DOI: 10.1016/j.idairyj.2003.11.005
LEE, C. H. et al. A coating for use as an antimicrobial and antioxidative packaging material incorporating nisin and a-tocopherol. Journal of Food Engineering, v. 62. p. 323-329. 2004. DOI: 10.1016/S0260-8774(03)00246-2
MARKIEWICZ-KESZYCKA et al. Fatty acid profile of milk - a review. Journal of Veterinary Research, v. 57, n. 2, p. 135-139, 2013. DOI: 10.2478/bvip-2013-0026
McGIBBON, A. K. H.; TAYLOR, M. W. Composition and structure of bovine milk lipids. In: FOX, P.F.; McSWEENEY, P. L. H. (ed.). Advanced Dairy Chemistry. Volume 2: Lipids. 3. ed. Nova Iorque: Springer, 2006.
MOYSSIADIA, T. et al. Effect of light transmittance and oxygen permeability of various packaging materials on keeping quality of low fat pasteurized milk: chemical and sensorial aspects. International Dairy Journal, v. 14. p. 429-436. 2004.
SALDANHA, T. et al. Capítulo 3: Lipídios. In: CRUZ, A. G. et al. (ed.). Química, Bioquímica, Análise Sensorial e Nutrição no Processamento de Leite e Derivados. Rio de Janeiro: Elsevier, 2016.
SMETA, K. et al. A change in antioxidative capacity as a measure of onset to oxidation in pasteurized milk. International Dairy Journal. v.18 p.520–530. 2008.
WASLTRA, P.; JENNESS, R. Química y Física Lactológica. Zaragoza: Editorial Acribia, 1984.
WALSTRA, P.; WOUTERS, J. T. M.; GEURTS, T. J. Dairy Science and Technology. 2. ed. Boca Raton: Taylor & Francis, 2006.
VASSILAA, E. et al. Chemical and microbiological changes in fluid milk as affected by packaging conditions. International Dairy Journal, v. 12. p. 715-722. 2002.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS