O período de transição é caracterizado como sendo das três semanas anteriores às três semanas posteriores ao parto e marca a mudança entre o estado de gestante não lactante para não gestante lactante.

Figura 1: Vaca recém-parida na maternidade. Nessa fase ocorrem grandes mudanças no metabolismo dos animais.
Podemos dizer, com convicção, que a alta incidência de doenças tanto metabólicas quanto infecciosas nesse período não acontecem por acaso, elas refletem os grandes desafios pelos quais os animais são submetidos nesse curto intervalo de tempo. São várias as mudanças pelas quais os animais devem passar e se adaptar adequadamente para que possam se manter saudáveis e produtivos. Podemos citar mudanças de manejo, nutrição, ressocialização, alterações endócrinas (hormonais), queda no consumo de alimentos próximo ao parto, balanço energético negativo com consequente mobilização de lipídeos (gordura), aumento das concentrações de ácidos graxos não esterificados na circulação sanguínea e de triglicerídeos no fígado, aumento da mobilização de proteína e aumento da demanda nutricional para a produção de leite.
Essas mudanças que ocorrem durante o período de transição são reguladas por mecanismos homeostáticos e homeorréticos. Os autores Dale Bauman e W. Bruce Currie da universidade de Cornell, em 1980 definiram o processo de homeorrexia como sendo mudanças coordenadas no metabolismo para conseguir suprir novos estados fisiológicos, que normalmente não sofrem influência da nutrição ou fatores externos. Portanto, ela é a responsável pela adaptação do animal às diferentes fases ao longo da vida, por exemplo, na mudança de não gestante para gestante ou não lactante para lactante. A homeostase, por sua vez, pode ser definida como os processos de regulação para manter o equilíbrio metabólico em diferentes condições nutricionais ou ambientais, por exemplo, o controle da temperatura corporal e a regulação do pH sanguíneo. Estas formas de controle são importantes para garantir as funções biológicas essenciais, garantir a sobrevivência do recém-nascido (através da produção de leite) ou a reprodução.
Muitas dessas alterações são inevitáveis e fazem parte da fisiologia do período de transição para a adaptação ¬à nova condição de lactante, porém, as magnitudes destas alterações variam, sendo fatores importantes que determinam sua saúde e produtividade da vaca até o fim da lactação. O desequilíbrio entre os processos homeorréticos e homestaticos causam problemas metabólicos como hipocalcemia, cetose, queda da imunidade predispondo o animal a infecções e fígado gorduroso.
Essas doenças ocorrem como um complexo pela grande relação entre suas etiologias e patogenias. A ocorrência desses problemas pode facilmente acabar com toda a expectativa de produção de uma vaca durante o restante da lactação, além de aumentar gastos com tratamento veterinário e a perda do potencial de produção do animal.
Uma ocorrência pelo qual todas as vacas passam é a queda no consumo voluntário, principalmente na semana que antecede o parto. Até o dia do parto, essa queda é de aproximadamente 30%, porém pode ocorrer uma grande variação, pois além de existir uma grande diferença individual, o meio no qual o animal se encontra pode influenciar fortemente agravando ou amenizando essa diminuição no consumo. Paradoxalmente, essa queda de ingestão de alimentos pela vaca ocorre quando a sua necessidade de nutrientes está crescendo de forma exponencial. Enquanto a vaca não conseguir suprir todas as suas necessidades nutricionais com o que ela absorve através da dieta, ela se encontra em um estado chamado de balanço energético negativo (BEN).
Durante o periparto, como estratégia evolutiva e que exacerbarmos as selecionar animais com grandes produções leiteiras, ocorre o desacoplamento do eixo somatotrópico com aumento da concentração de hormônio do crescimento (GH) e queda nos níveis do fator semelhante à insulina (IGF) -1. Além do aumento do GH, a baixa concentração de insulina e a resistência do organismo a responder ao seu estímulo favorecem o aumento da lipólise e da gliconeogênese hepática. Isso possibilita que haja maior disponibilidade de glicose para o feto no final da gestação e para a glândula mamária. Isso é possível porque a glândula mamária é um tecido insulina independente, ou seja, não necessita de insulina para captar a glicose sanguínea.
No caso da vaca em lactação, enquanto existir baixos níveis de insulina e uma resistência a sua atividade, a glândula mamária é favorecida, pois haverá menor disputa pelos nutrientes. Nesse cenário, outros tecidos passam a utilizar principalmente corpos cetônicos para suprir suas necessidades. Nesse mesmo período, são observadas altas concentrações de glucagon. Esse perfil hormonal com altas concentrações de GH, baixas concentrações de insulina e altas de glucagon representam um estado fisiológico de catabolismo, no qual ocorre a mobilização de reservas corporais como gordura corporal armazenada na forma de tecido adiposo e de proteína do tecido muscular.
Tabela 1: Mudanças metabólicas mais importantes associadas ao período de transição (adaptado de Ingvarsten, 2006).

Como dito anteriormente, durante o período de transição, o balanço energético negativo é esperado, porém quando este estado é exacerbado por desafios ambientais, predispõe o animal a doenças metabólicas e infecciosas que ocorrem de uma forma integrada.
Existem alguns outros fatores estressantes que podem aumentar o déficit entre energia utilizada e energia consumida aumentando o balanço energético negativo. São estes fatores que devem ser evitados ou pelo menos avaliados e monitorados para minimizar o balanço energético negativo. Alguns exemplos são: qualidade e disponibilidade do alimento, condições climáticas adversas como stress calórico, presença de ectoparasitas, claudicação, composição e forma de fornecimento da dieta pré e pós-parto, tamanho do cocho, ordem de lactação, duração do período seco, estresse provocado por ressocialização, locais de confinamento, aumento da frequência de ordenha, administração exógena de somatotropina, doenças infecciosas e metabólicas que podem diminuir o apetite e aumentar as necessidades nutricionais pela resposta imunológica produzida.
O fígado desempenha um papel chave na coordenação do fluxo de nutrientes para suprir as exigências do organismo. Esse órgão tem a função de reconhecer as necessidades nutricionais de todos os outros tecidos e responder ajustando o seu metabolismo. Após o parto, para conseguir suprir todas as necessidades do organismo, o metabolismo hepático aumenta imensamente, seguindo o aumento da produção de leite e do consumo de energia metabolizável. A produção de glicose pelo fígado mais do que dobra aos 11 dias pós-parto comparado aos 19 dias pré-parto, demonstrando um enorme aumento da gliconeogênese hepática.
O principal mecanismo homeorrético que ocorre no metabolismo lipídico na lactação é a mobilização de gordura corporal para suprir as exigências energéticas impostas pela nova condição de lactante. Essa mobilização ocorre principalmente durante o início da lactação. A mobilização do tecido adiposo acontece com a quebra de moléculas de triglicerídeos (TG) liberando ácidos graxos não esterificados (AGNE) e glicerol. Os AGNE são utilizados pelo organismo de várias formas, sendo as principais o seu uso pela glândula mamária para produção de parte da gordura do leite principalmente nos primeiros dias de lactação, pelo tecido muscular esquelético que o utiliza como fonte de energia e ainda, pode ser metabolizado no fígado em outros compostos.
A liberação de AGNE na corrente sanguínea aumenta proporcionalmente ao desequilíbrio entre a energia fornecida pelo consumo de alimentos e a energia requerida pelo organismo. Essa relação inversa entre a concentração sanguínea de AGNE e a ingestão de alimentos, o torna um bom marcador do balanço energético negativo, sendo capaz de determinar a sua intensidade e a adaptação do organismo a ele, refletindo a magnitude de mobilização das reservas corporais tanto pré como pós-parto. A concentração plasmática de AGNE começa a aumentar de dois a quatro dias antes do parto, porém em animais com risco de desordens metabólicas pode começar a aumentar mais cedo. O pico normalmente ocorre aproximadamente três dias após o parto.
Parte dos AGNE presentes na circulação são levados até o fígado, onde eles podem ser metabolizados de três formas: oxidados completamente produzindo CO2, água e ATP, o que disponibiliza energia para o órgão na forma da molécula do ATP; oxidados de forma incompleta gerando corpos cetônicos ou reesterificados para formar triglicerídeos. Os corpos cetônicos produzidos pela oxidação incompleta são principalmente o beta-hidroxibutirato (BHB), acetoacetato e cetona. O BHB é o corpo cetônico circulante predominante nos ruminantes e possui maior estabilidade na amostra de sangue em relação aos outros dois. Devido a essas características, a concentração plasmática de BHB reflete a ocorrência ou não da completa oxidação dos AGNE no fígado, demonstrando a capacidade deste órgão em metabolizar os AGNE liberados na circulação.
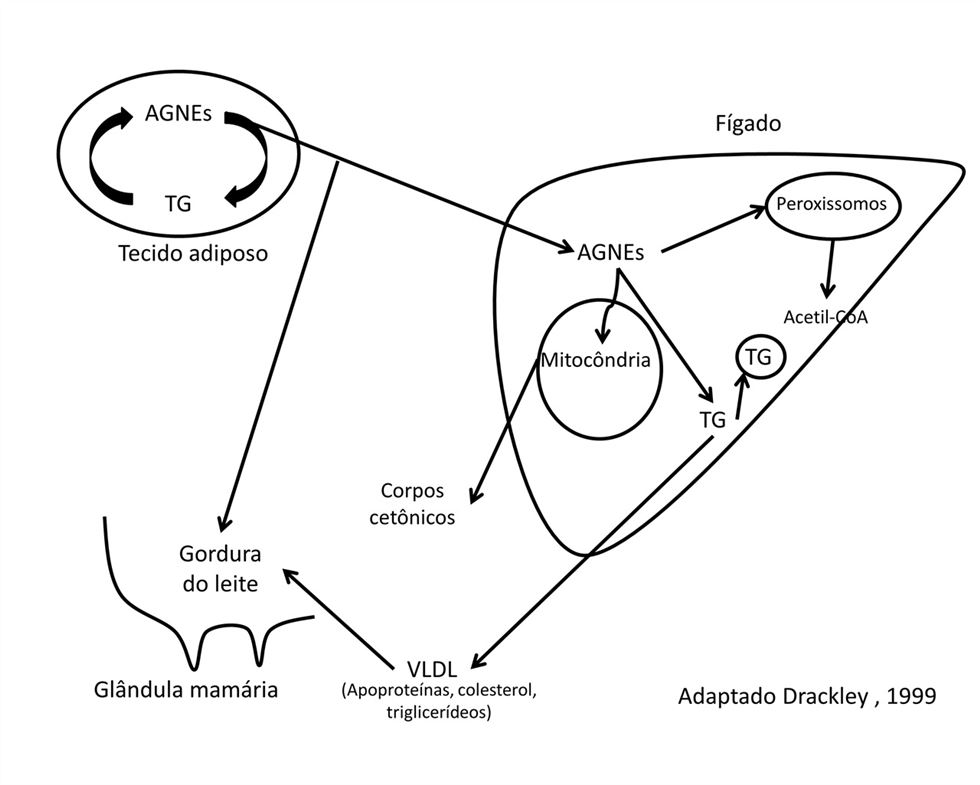
Figura 2: Esquema representando diferentes vias metabólicas do metabolismo lipídico durante o período de transição. TG = triglicerídeos; AGNEs = ácidos graxos não esterificados; VLDL = lipoproteínas de muito baixa densidade.
No período de transição, a síntese e elevação da concentração de corpos cetônicos é um importante mecanismo e até certo ponto um processo normal de adaptação metabólica para suprir as exigências da vaca no início de lactação, pois vários tecidos podem utiliza-los como fonte energética e também servem como precursores da gordura do leite, porém o seu excesso é anormal e patológico. A alta concentração dos corpos cetônicos no sangue é responsável pelo quadro de cetose, o qual poderíamos classificar como sendo clínica ou subclínica. A definição de cetose subclínica em gado de leite é o excesso de corpos cetônicos circulantes sem que haja sintomas clínicos e é diagnosticada quando a concentração plasmática de BHB é superior a 1,2 mmol/L.
As concentrações aumentadas tanto de AGNE como de BHB estão associadas com maiores risco de desenvolvimento de várias doenças como cetose, fígado gorduroso, deslocamento de abomaso, metrite, retenção de placenta, mastite, queda no desempenho reprodutivo, diminuição do status imunológico, aumento da chance de descarte e queda dos resultados de produção.
Os triglicerídeos formados no fígado pela reesterificação dos AGNE podem ser armazenados ou exportados pela circulação sanguínea a outros tecidos. Os ruminantes tem uma capacidade limitada de exportar os triglicerídeos formados através de moléculas de VLDL. O acúmulo de triglicerídeos no fígado causa um prejuízo a atividade normal do órgão, sendo essa patologia conhecida pelos nomes de esteatose hepática, fígado gorduroso ou lipidose hepática.








