Para ler a primeira parte do artigo, clique aqui.
Mecanismos que vinculam GH, insulino e IFG1 com a função do ovário
A maioria dos trabalhos que vinculam a nutrição com o crescimento folicular tem como foco o GH, a insulina e o IGF1. As células da granulosa, células tecais e lúteas metabolizam a glicose, mas há poucos trabalhos publicados sobre o papel da glicose na função normal dessas células. O desenvolvimento folicular é controlado por gonadotrofinas hipofisárias (LH e FSH). O controle do desenvolvimento folicular por LH e FSH depende das concentrações dos seus respectivos receptores e, também, da função dos sistemas do segundo mensageiro que, fundamentalmente determinam as respostas celulares. Nas vacas o desenvolvimento folicular começa logo após o parto, com aumento transitório de FSH, uma nova onda folicular e o desenvolvimento de um folículo dominante. A secreção pulsátil de LH determina se o folículo dominante irá ovular, transformar-se em cisto ou sofrer turn-over (falha na ovulação) (Beam e Butler, 1998).
As concentrações de insulina e IGF1 encontram-se inicialmente baixas, mas aumentam gradualmente no pós-parto (Lucy, 2003). Vacas com baixa condição corporal ou vacas que não melhoram sua condição corporal durante a lactação apresentam IGF1 sanguíneo baixo porque seu eixo somatotrópico permanece desacoplado (Lucy, 2007). Nossa hipótese é que as mudanças induzidas pela nutrição na secreção do IGF1 no fígado afetam diretamente o ovário, através das ações endócrinas do IGF1 (Figura 2). As concentrações mais baixas de insulina e IGF1, teoricamente, reduzem a resposta do ovário ao LH e FSH porque há relação sinérgica entre IGF1, insulina, LH e FSH, para o crescimento do folículo (Lucy, 2000; Webb et al., 2004).
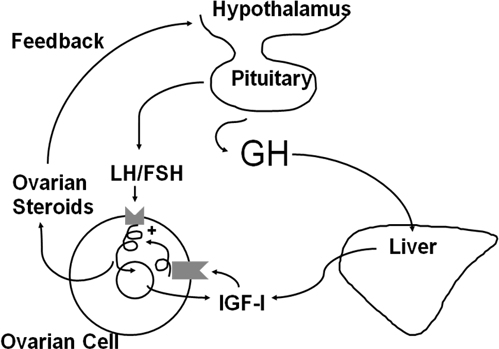
Figura 2. O vínculo entre o eixo somatotrópico e a função do ovário em vacas leiteiras. O hormônio do crescimento (GH) é produzido pela pituitária e atua no fígado para provocar a síntese e secreção do IGF1. O IGF1 atua sobre o ovário e, em sinergia com LH e FSH, promove o desenvolvimento do ovário e a produção de esteróides. Os esteróides (estradiol e progesterona) são essenciais para a reprodução normal.
Vacas com balanço energético negativo secretam menos IGF1 em resposta ao GH porque o eixo está desacoplado no fígado. O IGF1 mais baixo pode reduzir a resposta do ovário às gonadotrofinas.
A glicose e a insulina controlam o crescimento do concepto?
Recentemente foi concluído um estudo, no qual as vacas foram ordenhadas normalmente ou não ordenhadas, imediatamente após a parição (Green et al., 2009). As vacas foram inseminadas com aproximadamente 60 dias pós-parto, e o feto e a placenta foram coletados nos dias 28, 35 ou 42. A principal conclusão desse trabalho foi que, para um dia específico de gestação, o feto e a placenta de uma vaca em lactação eram menores que o feto e a placenta de uma vaca fora da lactação. Concluímos assim que a condição metabólica da lactação compromete (desacelera) o desenvolvimento do feto e da placenta. Uma possibilidade seria que essa taxa mais lenta de desenvolvimento levasse à perda embrionária nas vacas em lactação (perdem-se os embriões porque não alcançam as fases de desenvolvimento no seu devido tempo).
Do ponto de vista metabólico, as vacas em lactação diferem das vacas secas. De acordo com nossa análise, e também com o conhecimento atual sobre desenvolvimento fetal e placentário, a glicose e a insulina são os principais fatores que explicam o crescimento mais lento de embriões em vacas em lactação. A glicose é normalmente considerada uma fonte chave de energia para a produção de ATP através da fosforilação oxidativa mitocondrial. Entretanto, no embrião, a glicose é utilizada para a biomassa (nucleotídeos, aminoácidos, lipídeos, etc.) para a formação de novas células. Esse fenômeno recebe o nome de 'Efeito Warburg' e tipifica as células proliferativas. Assim, a glicose é o principal fator que impulsiona o desenvolvimento fetal e placentário.
A insulina pode ter um papel no processo, no sentido que a placenta e o útero expressam Glut4 (transportador de glicose insulino-dependente), embora a literatura geralmente indique que o Glut3 (não insulino-dependente) é o transportador da glicose mais crítico para o desenvolvimento fetal e placentário. Também se encontra na literatura a noção que a capacidade do útero e da placenta para transportar glicose geralmente não limita o desenvolvimento da gestação. Esse conceito está alinhado com os achados de Missouri, onde aparentemente os metabólitos produzidos fora do útero impulsionam o processo de desenvolvimento e crescimento fetal. Reduzir as concentrações de glicose sistêmica utilizando a lactação desacelera o desenvolvimento do feto e da placenta.
O trato reprodutor (especialmente o feto e a placenta) depende do meio metabólico (principalmente a glicose) da vaca. A glicose aparece como um metabólito importante que promove o desenvolvimento embrionário inicial. Acreditamos que baixas concentrações de glicose das vacas no pós-parto podem predispor o animal à perda do embrião porque a placenta poderá não ter o substrato adequado para a criação de novas células (biomassa). Uma placenta incompetente e com desenvolvimento lento poderá comprometer o embrião. Após a morte do embrião a placenta também morre e o corpo lúteo regride.
A glicose é um metabolito crítico para a vaca em lactação e para a gestação. Resulta interessante que seu propósito, tanto na glândula mamária quanto na gestação não é a produção de combustível metabólico (i.e. a glicose não é utilizada para produzir ATP). Na glândula mamária, a maior parte da glicose é utilizada para produzir lactose (açúcar do leite). Da mesma forma, no útero e na placenta, a maior parte da glicose é utilizada para produzir células novas (biomassa).
Assim, tanto para a glândula mamária quanto para a gestação é necessária a presença de glicose. A glândula mamária possui a capacidade de sequestrar grandes quantidades de glicose através do transportador passivo Glut1, diferentemente dos dois transportadores passivos Glut 1 e Glut3 utilizados pelo útero e a placenta. De qualquer forma, a disponibilidade de glicose aparentemente também impulsiona a capacidade de produção de leite. Em nosso ensaio, as concentrações de glicose no sangue durante o primeiro mês pós-parto eram inferiores em vacas que não ficaram prenhes na primeira inseminação (aproximadamente 60 días após o parto). Foi interessante observar que essas mesmas vacas, com níveis mais baixos de glicose no sangue, também apresentaram produção mais baixa de leite. Com base nesses dados, aparentemente a capacidade da vaca para produzir glicose através da gliconeogênese no fígado determina sua capacidade para produzir leite porque a glicose é necessária para a síntese da lactose. A capacidade de produzir glicose pela gliconeogênese também pode determinar a capacidade da vaca de ficar prenhe porque, tanto a glândula mamária, quanto a gestação competem pelo mesmo substrato crítico (glicose).
A glândula mamária tem prioridade para a glicose, mas nem ela nem o útero/placenta tem a capacidade de concentrar glicose através de um transportador de glicose. Se isso for verdadeiro, por que a glândula mamária teria prioridade? Nossa hipótese é que o maior fluxo sanguíneo para a glándula mamária determina sua maior capacidade para extrair glicose da circulação. O útero perde a batalha pela glicose porque seu fluxo sanguineo e capacidade para extrair glicose do sangue durante período inicial da gestação é menor que o fluxo sanguíneo e a capacidade da glândula mamária para extrair glicose.
Acreditamos que existe uma 'Barreira de Glicose' para o estabelecimento precoce da gestação. De acordo com os argumentos apresentados acima, como poderíamos transpor a 'Barreira de Glicose'? A primeira solução óbvia seria maximizar a saúde hepática dos animais em transição, de forma que o fígado tenha a capacidade de gerar glicose (o tecido hepático sadio deveria produzir mais glicose via gluconeogênese). Essa é a estratégia utilizada e comerzializada por algumas companhias (Colina rúmen protegida, por exemplo). A segunda possibilidade seria manipular a curva de lactação de forma que a disponibilidade de glicose fosse maior durante a fase inicial da lactação.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS











