O processo de encapsulamento é o método mais adequado para essa finalidade, sendo a técnica de spray drying a mais utilizada industrialmente. Entretanto, a alta temperatura aplicada nessa técnica pode ter um efeito negativo sob a viabilidade dos micro-organismos, sendo necessária a incorporação de um material de parede adequado. Os soros lácteos, devido a sua composição rica em lactose e proteínas, apresentam potencial para uso como agentes encapsulantes (ANAL; STEVENS, 2005).
Portanto, o objetivo desse trabalho foi encapsular L. plantarum ATCC 8014 por spray drying, utilizando soro de queijo, permeado e retentado de soro como materiais de parede.
Metodologia
As células bacterianas foram previamente incubadas em caldo MRS, lavadas e ressuspendidas em cada uma das soluções de alimentação. Estas foram microencapsuladas por spray drying, operando a temperatura constante, ar de entrada de 90ºC, ar de saída de 75°C, vazão de alimentação de 0,25 L.h-1 e vazão de ar de 2,5 m3.min-1. As amostras em pó das microcápsulas de soro de queijo (MS), microcápsulas de permeado (MP) e microcápsulas de retentado de soro (MR) foram recolhidas no ciclone e armazenadas em frascos estéreis a 20°C. A contagem de células viáveis de L. plantarum foi determinada antes e logo após o processo de spray drying e a sobrevivência do micro-organismo encapsulado foi avaliada ao longo de oito semanas.
Resultados e discussão
A Tabela 1 apresenta o número de células viáveis de L. plantarum ATCC 8014 antes e após o processo de spray drying.
Tabela 1. Viabilidade de L. plantarum ATCC 8014 antes e após spray drying.
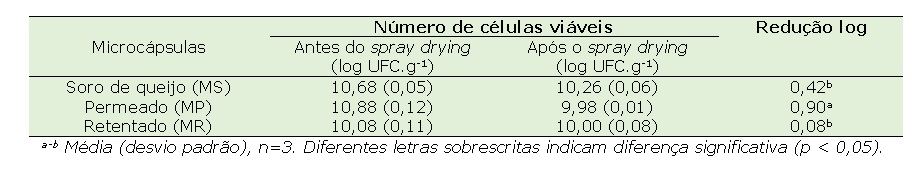
As MS e MR apresentaram resultados semelhantes após o encapsulamento, provavelmente pela similaridade da composição desses dois subprodutos lácteos. Já as MP apresentaram uma redução mais pronunciada na viabilidade celular. A proteção bacteriana no encapsulamento é adquirida principalmente pela interação entre proteínas e açúcares presentes nos subprodutos aplicados como materiais de parede. No caso do permeado, o seu principal constituinte é a lactose, sendo assim, a agregação das moléculas pode ser afetada, reduzindo o efeito protetor à célula (HUGO et al., 2016).
A Figura 1 apresenta a sobrevivência do L. plantarum encapsulado durante oito semanas. A temperatura de 20ºC foi escolhida porque é a maneira mais econômica para o armazenamento de produtos secos.
Figura 1. Viabilidade das microcápsulas durante 56 dias de armazenamento.
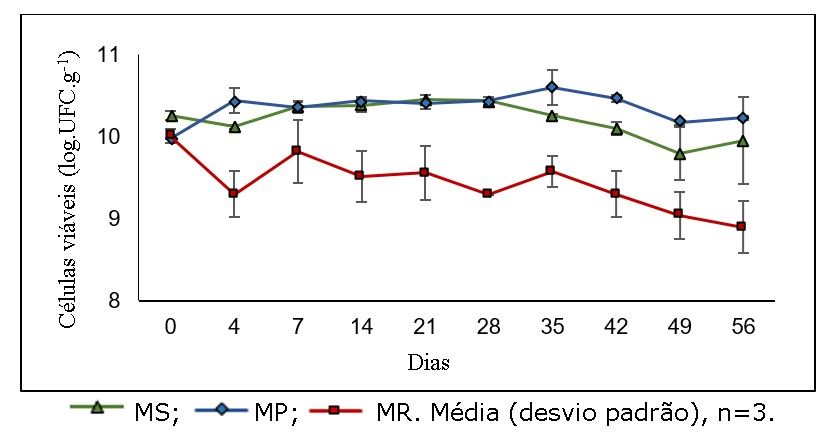
As MS e MP não apresentaram redução na viabilidade após o armazenamento a 20ºC, mas as MR apresentaram redução de 1,11 ciclos log após 56 dias. No entanto, todas as microcápsulas mantiveram uma contagem acima de 6 log.UFC.g-1, que é a quantidade mínima exigida de bactérias probióticas em alimentos funcionais (FAO/WHO, 2002).
Os soros lácteos são uma fonte alternativa e rentável da obtenção de proteínas e açúcares, e de acordo com os resultados, são adequados no uso como materiais encapsulantes. Porém, na maioria dos trabalhos são combinados com outros agentes protetores (PINTO et al., 2015; HUGO et al., 2016). Esse estudo demonstrou que os soros oriundos das indústrias de laticínios podem ser aplicados no encapsulamento de bactérias lácticas por spray drying, sem a necessidade de outro agente protetor.
Referências bibliográficas
Anal, A. K.; Stevens, W. F. 2005. Chitosan-alginate multilayer beads for controlled release of ampicillin. International Journal of Pharmaceutics. 290:45-54.
FAO/WHO. 2002. Gidelines for the evaluation of probiotics in food. Report of a Joint FAO/WHO working group on drafting guidelines for the evaluation of probiotics in food. Food and Agriculture Organization of the United Nations/World Health Organization. London, Ontario, Canada.
Hugo, A. A.; Bruno, F.; Golowczyc, M. A. 2016. Whey permeate containing galacto-oligosaccharides as a medium for biomass production and spray drying of Lactobacillus plantarum CIDCA 83114. LWT-Food Science and Technology. 69:185-190.
Martín, M. J.; Villoslada, F. L.; Ruiz, M. A.; Morales, M. E. 2015. Microencapsulation of bacteria: A review of different technologies and their impact on the probiotic effects. Innovative Food Science and Emerging Technologies. 27:15-25.
Pinto, S. S.; Fritzen-Freire, C. B.; Benedetti, S.; Murakami, F. S.; Petrus, J. C. C.; Prudêncio, E. S.; Amboni, R. D. M. C. 2015. Potential use of whey concentrate and prebiotics as carrier agents to protect Bifidobacterium BB 12 microencapsulated by spray drying. Food Research International. 67:400-408.
Soccol, C.R.; Vandenberghe, L. P. S.; Spier, M.R.; Medeiros, A. B. P.; Yamaguishi, C.T.; Lindner, J. D.; Pandey, A.; Thomaz-Soccol, V. 2010. The Potential of Probiotics: A Review. Food Technology Biotechnology. 48:413-434.
Vanderpool, C.; Yan, F.; Polk, D. B. 2008. Mechanisms of probiotic action: implications for therapeutic applications in inflammatory bowel diseases. Inflammatory Bowel Diseases. 14:1585-1596.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS















