Bactérias lácticas compreendem um grupo de microrganismos que habitam o trato gastrintestinal (TGI) humano, onde representam a microbiota dominante do intestino delgado (Jensen et al., 2012). Essas bactérias podem causar efeitos benéficos ao hospedeiro, devido à capacidade de colonizar o TGI e promover o equilíbrio da microbiota, além de fornecer uma barreira contra patógenos e modular o sistema imune auxiliando na prevenção de doenças (Sarkar e Mandal, 2016).
Para isso, devem resistir as enzimas digestivas, aos baixos níveis de pH do suco gástrico e aos sais biliares do intestino (Martín et al., 2015). Entretanto, essas bactérias podem apresentar limitada resistência a essas condições, necessitando de uma barreira externa como proteção. Para essa finalidade, o encapsulamento por meio do processo de spray drying é a tecnologia mais utilizada industrialmente. Além disso, os subprodutos da indústria de laticínios são uma alternativa como material encapsulante, uma vez que conferem proteção aos microrganismos (Ilha et al., 2015).
Portanto, o objetivo desse trabalho foi avaliar bioencapsulados de Lactobacillus plantarum ATCC 8014, produzidos por spray drying, com soro de queijo, permeado ou retentado de soro como agentes encapsulantes, quanto à resistência ao TGI simulado.
Metodologia
As microcápsulas foram armazenadas a 20ºC e então expostas as soluções gastrintestinais simuladas em 0 e 28 dias. Suco gástrico, contendo 3,0 mg.mL-1 de pepsina, 0,5% (m/v) de NaCl, a pH 2,0, 2,5 e 3,0. Suco intestinal, contendo 1,0 mg.mL-1 de pancreatina, 0,5% (m/v) de NaCl a pH 8,0, com ou sem 5,0 g.L-1 de uma mistura 1:1 de colato de sódio e deoxicolato de sódio. As contagens de células viáveis foram determinadas após 3 horas para trato gástrico e 4 horas para trato intestinal.
Resultados e discussão
A viabilidade das microcápsulas de L. plantarum ATCC 8014 expostas ao TGI simulado está apresentada na Figura 1.
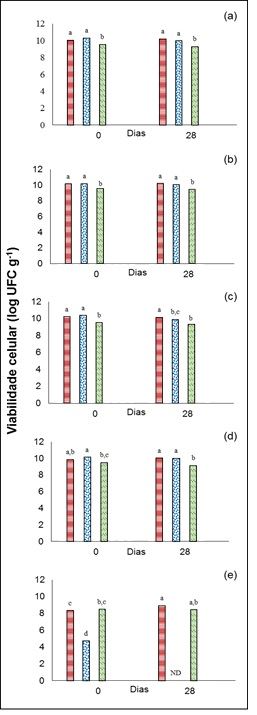
Para trato gástrico (Figuras 1. a,b,c) em todas as condições avaliadas a viabilidade dos encapsulados manteve-se elevada e semelhante a concentração bacteriana inicial (9,30-10,20 log UFC.g-1). A presença de pepsina e os diferentes pHs nos quais as microcápsulas foram expostas não afetou a viabilidade das células do microrganismo L. plantarum ATCC 8014.
Para trato intestinal (Figuras 1. d,e), na presença de pancreatina todas as microcápsulas apresentaram viabilidade celular superior a 8,0 log UFC.g-1. No geral, enzimas digestivas, tais como pepsina e pancreatina, embora consideradas danosas para o microrganismo, têm menos influência sobre a viabilidade das bactérias, enquanto os baixos valores de pH e a concentração de sais biliares são considerados fatores críticos (Ranadheera et al., 2014). Entretanto, observou-se que a principal perda de viabilidade ocorreu na presença de 0,5% (m/v) de sais biliares para microcápsulas de permeado. Neste caso, no tempo inicial foi observada redução de 5 log UFC.mL-1 e após 28 dias de armazenamento o L. plantarum ATCC 8014 bioencapsulado com permeado não sobreviveu a essa concentração de sais biliares.
Estes resultados podem ser associados com a composição físico-química dos subprodutos aplicados como agentes encapsulantes. O permeado de soro tem um menor teor de proteínas em sua composição, sendo constituído, principalmente, por lactose, o que reduz o seu efeito protetor (Maciel et al., 2014).
O L. plantarum ATCC 8014 não encapsulado, quando comparado com as células bioencapsuladas, apresentou uma menor tolerância ao TGI simulado. Para trato gástrico, no pH 2,0 não apresentou sobrevivência, enquanto para pHs 2,5 e 3,0 uma redução de 5,0 e 1,9 ciclos log, respectivamente, foi observada.
Para trato intestinal, a contagem de células manteve-se inalterada na ausência de 0,5% (m/v) de sais biliares, mas na presença, observou-se uma redução de 0,67 log. Estes resultados indicam que o microencapsulamento com soros lácteos, principalmente com soro de queijo, resulta num ambiente adequado para a proteção ao TGI simulado do microrganismo L. plantarum ATCC 8014.
Referências bibliográficas
ILHA, E. C.; SILVA, T.; LORENZ, J. G.; ROCHA, G. O.; SANT’ANNA, E. S. Lactobacillus paracasei isolated from grape sourdough: acid, bile, salt, and heat tolerance after spray drying with skim milk and cheese whey. European Food Research Technology. v. 240, p. 977-984, 2015.
JENSEN, H.; GRIMMER, S.; NATERSTAD, K.; AXELSSON, L. In vitro testing of commercial and potential probiotic lactic acid bactéria. International Journal of Food Microbiology. v. 153, p. 216-222, 2012.
MACIEL, G. M.; CHAVES, K. S.; GROSSO, C. R. F.; GIGANTE, M. L. Microencapsulation of Lactobacillus acidophilus La-5 by spray-drying using sweet whey and skim milk as encapsulating materials. Journal of Dairy Science. v. 97, p. 1991-1998, 2014.
MARTÍN, M. J.; VILLOSLADA, F. L.; RUIZ, M. A.; MORALES, M. E. Microencapsulation of bacteria: A review of different technologies and their impact on the probiotic effects. Innovative Food Science and Emerging Technologies. v. 27, p. 15-25, 2015.
RANADHEERA, C. S.; EVANS, C. A.; ADAMS, M. C.; BAINES, S. K. Effect of dairy probiotic combinations on in vitro gastrointestinal tolerance, intestinal epitelial cell adhesion and cytokine secretion. Journal of Functional Foods. v. 8, p.18-25, 2014.
SARKAR, A.; MANDAL, S. Bifidobacteria - Insight into clinical outcomes and mechanisms of its probiotic action. Microbiological Research, v. 192, p. 159-171, 2016.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
















