A técnica de contagem de larvas no pasto tem como finalidade à determinação quantitativa e qualitativa de larvas na forma infectante (L3 e algumas formas imaturas) das espécies aos quais os animais de fazenda estão expostos.
Embora o exame de amostragem de pasto seja pouco utilizado, este demonstra dados que podem complementar o exame coprológico, auxiliando um programa de controle integrado. A utilidade epidemiológica prática é considerada importante e somente com este tipo de técnica é que foi determinado que o desenvolvimento de ovos até L3 do Haemonchus spp. e do Trichostrongylus spp , no meio ambiente, ocorre dentro de uma semana e que o estádio infectante sobrevive por até 12 e 10 semanas, respectivamente.

Figura 1. Presença de inúmeras larvas contidas em uma pequena gota de orvalho em um ramo de pasto.
As variações do clima, assim como o manejo da propriedade e do terreno, deve ser considerado no momento da amostragem do pasto para uma melhor interpretação dos resultados. O clima determina quais os nematodas podem ser encontrados em um determinado local, enquanto que as variáveis atmosféricas são responsáveis por determinar quais destes podem se desenvolver e infectar os hospedeiros.
Existe um aumento na ocorrência de larvas infectantes durante o outono e inverno. Estas estações do ano influenciam a epidemiologia de parasitas gastrintestinais em ovinos. A sobrevivência (acima de 2 meses) do Haemonchus placei, Cooperia spp. e Oesophagostomum radiatum é alta sob clima tropical com inverno seco e verão chuvoso.
O índice de pluviosidade é considerado a condição climática de maior importância, afetando o desenvolvimento e a sobrevivência das larvas de nematodas na pastagem. Foi determinado também que pode haver maior eliminação de larvas do bolo fecal durante períodos de chuva amena. Foi descrito que existe uma interação entre o aumento do índice pluviométrico e o alto índice de infecções de helmintos em animais jovens. Ovos inoculados em pastagens durante a seca apresentam uma redução significativa de eclodibilidade e o bolo fecal de animais depositado na época da seca, forma uma carapaça que inibe a migração das larvas, mas favorece a sobrevivência das mesmas, permanecendo estes positivos para larvas infectantes por um período prolongado.
Muito embora as baixas temperaturas possam alterar a viabilidade das larvas, retardando seu desenvolvimento, mesmo o inverno rigoroso não impede que algumas larvas presentes no solo permaneçam viáveis para o próximo ano. A temperatura média ideal de desenvolvimento de larvas infectantes é de aproximadamente 17 ºC, porém temperaturas entre 14 e 32 ºC propiciam condições para sobrevivência de estádios pré-infectantes.
Diferenças de altitude também são fatores que podem alterar a obtenção de larvas. Deve-se fazer a amostragem preferencialmente na parte da manhã, evitando-se a colheita após o ressecamento da pastagem pelo sol. A umidade presente no solo e na pastagem neste horário previne a dissecação das larvas e sua morte.
Características de manejo e da pastagem na propriedade
Propriedades que desenvolvem algum esquema de rotação de pastagem com intervalo de até quatro meses e apresentam baixa lotação animal podem apresentar baixo grau de contaminação larval no pasto. Assim como o fato de que as larvas ficam relativamente perto do bolo fecal (principalmente para bovinos), a alta densidade animal pode ser determinante para uma alta taxa de infecção/transmissão.
Neste mesmo aspecto, um programa de rotação rápida das pastagens pode aumentar a taxa de transmissão forçando os animais a ingerir porções de pasto altamente contaminado. Opondo-se a isto, programas de rotação intensa podem provocar aumento da destruição do bolo fecal, devido ao pisoteio dos animais, provocando um aumento da dessecação das fezes e conseqüente destruição de ovos e larvas. Nestes dois casos deve-se estudar o equilíbrio entre altura da pastagem (disponibilidade proteína e fibra) e lotação animal.
O acesso de animais em áreas após a colheita (milho, sorgo, soja) assegura que os animais não terão contato com formas infectantes no novo local. Desta forma, os animais que forem colocados nestas áreas terão um menor risco de contaminação, significando também a diminuição da taxa de infestação do meio ambiente por estes animais. Entretanto, esta estratégia pode ser equivocada se os animais forem tratados com medicação antiparasitária de longa ação, o que aumentará a pressão de seleção para parasitas resistentes. É indicado que a mudança de animais para pasto "limpo" seja feita sem que haja o tratamento antiparasitário prévio. O objetivo desta estratégia é preservar a população de larvas em refugia e a vida útil dos compostos antiparasitários.
O tamanho dos piquetes é um fator importante, pois os animais podem estar condicionados em porções limitadas dentro de uma grande área. Então, a pastagem deve ser colhida preferencialmente de locais onde os animais mais ocupam o terreno, com uma única amostragem das outras áreas. A topografia do terreno é outro fator importante a ser considerado. Se o terreno for plano, deve-se proceder com a amostragem simples, no entanto se o terreno for desigual (declives moderado a alto) todas as áreas devem ser percorridas. Neste caso deve-se fragmentar os piquetes de acordo com a declividade topográfica e interpretar a contagem das larvas em separado.
O solo pode ter um efeito importante na capacidade de migração das larvas. Solos arenosos favorecem a migração das larvas para uma distância maior do bolo fecal, comparado com solos argilosos: menos de cinco larvas em 500 amostras. A diferença na taxa de migração de larvas para fora do bolo fecal entre locais com características de terreno seco e úmido é muito significativa. O solo úmido favorece a migração das larvas para fora do bolo (140 vs. 352 em uma grama no bolo fecal) em relação ao solo seco.
Tipo de parasita
Haemonchus sp., Oesophagostomum sp., Trichostrongylus sp., Ostertagia sp. e Cooperia sp. são parasitas que podem estar presentes por causa de sua maior oviposição, enquanto o Dictyocaulus spp. estará presente em pouca quantidade, principalmente no verão.
Ciclo biológico direto - exemplo: Haemonchus contortus
A vida de um nematódeo se inicia com a cópula entre machos e fêmeas no local de parasitismo, dentro do animal. As fêmeas realizam a postura de ovos que irão para o meio exterior com as fezes do animal. Esses ovos, encontrando condições propícias de umidade e temperatura, evoluem e passam a conter uma larva em seu interior (larva de primeiro estádio - L1). Quando completamente desenvolvida, passando pela fase de L2, a larva L3 sai do bolo fecal e se alimenta de microorganismos e matéria orgânica, presente no solo e na pastagem. Esta fase é chamada de forma infectante. Para prosseguir o seu desenvolvimento a L3 necessita ser ingerida pelo animal.
As larvas presentes no meio ambiente são bastante resistentes podendo permanecer por vários meses nas pastagens. Elas são móveis e são governadas pelo estímulo da umidade. Nas horas mais frescas do dia, elas se locomovem pela película de orvalho que recobre as vegetações indo a direção das partes mais altas das vegetações (5 cm em média).
Nas horas mais quentes e ensolaradas as larvas dirigem-se para as partes inferiores das plantas, chegando a penetrar na superfície do solo (até 25 cm no inverno) em busca de um ambiente mais propício para sua sobrevivência.
A umidade ótima para os ovos e larvas é de 80% e a temperatura entre 22 a 26 ºC. Temperaturas superiores a 30 ºC provocam um desenvolvimento mais rápido, porém, as larvas se tornam hipercinéticas (grande movimentação) e consomem rapidamente suas reservas e morrem mais rapidamente.
O animal adquire a infecção ao ingerir a larva infectante juntamente com o pasto. Dentro do organismo do animal, a larva evolui e cresce até atingir o estádio adulto, onde machos e fêmeas copulam, fechando o ciclo.
Métodos de amostragem
Sugere-se colher amostras cobrindo uma grande área, utilizando uma amostragem em zigue-zague. Deve-se então proceder com o corte rasteiro do pasto, colocando o material (aprox. 600g) em sacos plásticos e uma pequena amostra para determinação de matéria seca.
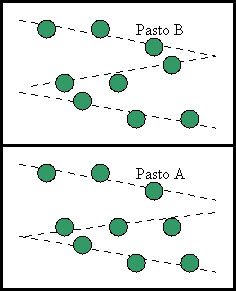
Figura 2. Forma de amostragem de pasto em zigue-zague. O correto é colher amostras de todos os piquetes, relatando o histórico de ocupação das parcelas.
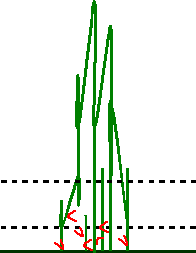
Figura 3. Deve-se colher amostras de pasto em altura abaixo de 3 cm, podendo descartar o material acima de 15cm. Assim será possível obter uma amostragem significativa de larvas e que facilitará a interpretação dos achados.
Técnica de lavagem de pasto
O procedimento se inicia com a lavagem do pasto em água separando as fibras e retornando-as para o meio. Após três horas o material é retirado para então ser peneirado para remoção de partículas. As larvas ficarão retidas em outra fase de separação para identificação zoológica com auxílio de microscópio.
Mesmo com todo este trabalho, acredita-se que o percentual médio de obtenção das larvas seja de aproximadamente 20 a 40%. A contagem final se baseia no número de larvas por quilo de matéria seca. Deve-se utilizar um fator de correção para este processo: 100/número de larvas recuperadas em um quilo, devendo este ficar próximo de 6,7. Pastagens com valores acima de 1.000 L3/kg/MS de trichostrongilídeos, são consideradas moderadamente infectadas, enquanto que contagens acima de 5.000 L3/kg podem indicar a presença de infecção clínica em animais jovens.
Então, depois de analisadas todas as variáveis, o técnico dispõe de mais uma grande fonte de informação epidemiológica. Como esperado estes números poderão sofrer grande variação ao longo do ano para cada região, devido à flutuação da ocorrência dos parasitas.
Manejo seletivo (TST: target selected treatment): A preocupação do aumento de larvas no pasto e o equilíbrio intra-espécie (ou intra-rebanho)
Nestes tempos difíceis, onde os relatos da falha na eficácia dos produtos antiparasitários são cada vez mais comuns, o tratamento seletivo do rebanho vem recebendo uma atenção especial. Os resultados positivos com a utilização do método Famacha e/ou escore corporal e a OPG como forma de selecionar animais em duas categorias; susceptíveis: tratados e os tolerantes: não-tratados, sugere que a manutenção de indivíduos contaminados no rebanho não só seja necessária como fundamental para a manutenção da eficácia dos produtos. E isto realmente é muito importante!
Contudo, um dos primeiros questionamentos é quanto ao aumento do número de larvas que serão depositadas no pasto pelo grupo de animais não-tratados. Caso este número seja pequeno, menor do que 2%, o percentual de incremento de larvas apresentará pouca influência na distribuição da carga parasitaria. Entretanto, os dados atuais no Brasil indicam que quando a estratégia de TST é utilizada, o percentual de animais não-tratados pode chegar a mais de 90%. Neste caso o volume de larvas depositadas na pastagem será enormemente maior.
Tabela 1. Número de animais por categoria Famacha e percentual de ovinos da raça Texel e Ile de France tratados com medicação antiparasitária nos anos de 2003 a 2006. Rebanho da Universidade Federal de Santa Maria, RS.
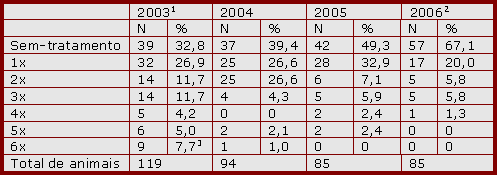
1: Realizado dois tratamentos táticos em janeiro e março; 2: Período entre janeiro a julho; 3: Incluindo a soma de animais que receberam 6, 7 e 8 tratamentos (Gavião e Molento, manuscrito em preparação).
Os técnicos de campo e produtores sabem da capacidade dos animais em suportar períodos adversos. Isto ocorre também durante um ataque parasitário, sem que haja prejuízo zootécnico para uma vasta maioria dos animais. Obviamente, respeitando aqueles períodos de infecção aguda ou de surtos parasitários. Ocorre que a utilização de esquemas de tratamento antiparasitário preventivo/supressivo é tão grande que, neste caso, existe uma supressão da resposta imune do animal.
Para contrabalancear a necessidade do tratamento constante poder-se-ia fazer uma pergunta simples: "Será que sai caro para o organismo do animal ser tolerante, isto é, defender-se com seus próprios meios?" Na verdade não. O que a ciência sabe é que existem vários mecanismos, internos e externos, que atuam neste momento formando uma barreira: sistema imune, bioquímica, comportamento, histórico do animal e a estrutura, que reconhecem o momento do ataque. Estas formas de resposta podem apresentar dano (ou custo) ao animal caso este seja do grupo susceptível ou não, caso os animais pertençam ao grupo resistente/resiliente.
Confirmando estas afirmações, os dados de campo ao longo destes últimos quatro anos sugerem que exista uma forte resposta dos animais (intra-espécie) que compõem o rebanho para equilibrar a taxa de sucesso das larvas e a quantidade de ovos depositados por cada fêmea adulta no meio ambiente. Este fato sugere que caso haja uma grande taxa de contaminação em um primeiro momento, o próprio rebanho poderá estabilizar o numero de parasitas disponíveis. É fundamental então que os profissionais devam se atualizar sobre programas como o TST ou SICOPA para propor estratégias integradas de controle parasitário de longo prazo.
Conclusão
A finalidade de utilizar a lavagem de pasto como ferramenta para a parasitologia possibilita a obtenção de informações quantitativas sobre os gêneros presentes (larvas/kg.MS) e o estudo da dinâmica destas populações. Muito embora alguns estudos tenham comprovado que o número médio de vermes adultos encontrados em ovinos é correspondente ao índice de larvas infectantes nas pastagens, a interpretação de qualquer resultado obtido através de uma única amostragem deve ser precedida de muita cautela. Devem ser feitas considerações sobre os inúmeros fatores que podem influenciar no resultado para daí então propor uma estratégia de controle parasitário efetivo.
Os resultados provenientes do exame das pastagens, juntamente com o conhecimento de dados provenientes do exame de fezes e necropsia, podem fornecer subsídio valioso para o profissional empenhado em compreender e melhorar as condições dos rebanhos e em ampliar o conhecimento da dinâmica de infecção parasitária em ruminantes. Proprietários e técnicos devem estar atentos a este detalhe e dar a devida importância quando forem indicar estratégias como o TST/SICOPA e prescrever as recomendações de controle parasitário.

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS












