O leite é um alimento de reconhecido valor nutricional por apresentar em sua composição elevada concentração de cálcio e proteínas de valor biológico, além de peptídeos bioativos com ação protetora na saúde humana, tais como antibacteriana, antiviral, antifúngica, antioxidante, anti-hipertensiva e antitrombótica (PEREIRA, 2014).
No entanto, a lactose presente no leite limita o consumo desses produtos por indivíduos que apresentam intolerância à lactose. A intolerância a esse açúcar é devido à diminuição dos níveis da enzima β-galactosidase na parede intestinal. Segundo Mattar e Mazo (2010), no Brasil essa intolerância ocorre em 57% da população de cor branca, 80% dos indivíduos negros, chegando a 100% da população de origem japonesa.
Em virtude dessa problemática, a indústria de laticínios tem investido no desenvolvimento e na modificação de produtos à base de leite (FREITAS et al., 2011). A reação de hidrólise enzimática surge como um dos processos biotecnológicos mais importantes na indústria de alimentos, pelo efeito benéfico na assimilação da lactose, bem como uma possível vantagem tecnológica e ambiental de grande aplicação na indústria (GÜRDAS et al., 2012).
As β-galactosidases usadas em escala industrial devem ser provenientes de micro-organismos Generally Recognized as Safe (GRAS). As enzimas obtidas de fungos filamentosos (Aspergillus oryzae e Aspergillus niger) e de leveduras (Kluyveromyces lactis e Kluyveromyces fragilis) possuem grande potencial comercial.
Algumas características importantes para uso da enzima em processos industriais são o pH ótimo de atuação, a termoestabilidade e a elevada atividade enzimática a baixas temperaturas (HUSAIN, 2010).
Com base nisso, o objetivo desse trabalho foi estudar a hidrólise enzimática da lactose do leite empregando duas β-galactosidases comerciais de origem microbiana e avaliar a influência da concentração da enzima e da temperatura na reação.
Material e métodos
O leite em pó utilizado nos ensaios foi reconstituído a 5% (m/v) de lactose. Os processos de hidrólise enzimática foram realizados empregando concentrações de 3, 6 e 9 U/mL da β-galactosidase de Aspergillus oryzae ou de Kluyveromyces lactis nas temperaturas de 10 e 55°C para a enzima de A. oryzae e de 10 e 37°C para a β-galactosidase de K. lactis.
Após 0, 1, 2, 4, 8 e 12 horas de reação de hidrólise coletaram-se amostras que foram submetidas a aquecimento a 100°C em banho-maria por 10 minutos para inativação da enzima e após isso determinou-se a concentração de glicose por meio do kit enzimático Bioliquid.
A avaliação estatística foi realizada por Análise de Variância (ANOVA), e verificada a significância dos modelos pelo Teste-F. Nos modelos significativos, as médias foram comparadas entre si pelo Teste de Tukey, ao nível de 95% de significância (p<0,05) utilizando o software Bioestat 5.0.
Resultados e discussão
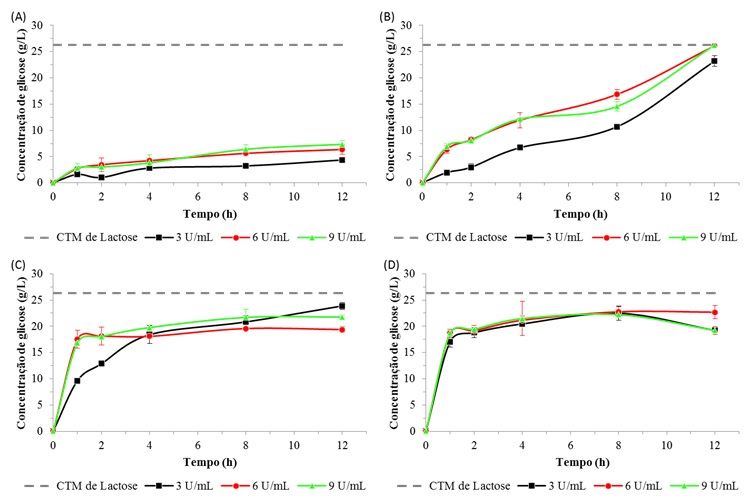
A Figura 1 apresenta os resultados de hidrólise da lactose do leite, pelas enzimas de A. oryzae e de K. lactis ao longo das 12 horas de reação.
Figura 1. Concentrações de glicose resultantes da hidrólise enzimática da lactose do leite pelas enzimas β-galactosidases de A. oryzae: (a) 10 °C, (b) 55 °C e de K. lactis: (c) 10 °C, (d) 37° C. A linha pontilhada em cada gráfico indica a concentração de glicose correspondente à conversão teórica máxima de lactose (CTM).
Comparando o processo de hidrólise a 10ºC e na temperatura ótima de cada uma das enzimas, verificou-se que, nas condições experimentais empregadas, o efeito da variação da temperatura foi mais expressivo para a β-galactosidase de A. oryzae do que para a β-galactosidase de K. lactis.
A Figura 1 mostra que a hidrólise da lactose do leite pela enzima de A. oryzae foi superior na temperatura ótima em relação à de 10°C, já para a enzima de K. lactis as concentrações de glicose geradas a partir da hidrólise da lactose são semelhantes em ambas as temperaturas testadas (10 e 37°C).
Em relação à concentração da enzima empregada no processo de hidrólise da lactose, verificou-se que a variação desse parâmetro teve uma maior influência quando utilizada a β-galactosidase de A. oryzae. Para a enzima de K. lactis, os resultados de hidrólise da lactose do leite foram semelhantes, independente da concentração testada.
Observa-se que para a β-galactosidase de A. oryzae as concentrações de glicose aumentaram gradualmente ao longo de todo o período de hidrólise, atingindo em 12 horas, na temperatura ótima, valores próximos a máxima conversão teórica da lactose nos seus respectivos açúcares.
Enquanto que para a β-galactosidase de K. lactis verifica-se um aumento gradual da concentração de glicose nas primeiras duas horas de reação e após permaneceu praticamente constante ao longo do tempo de processo avaliado, atingindo valores de aproximadamente 20 g/L de glicose.
A Tabela 1 apresenta os resultados de eficiência de hidrólise da lactose do leite, pelas enzimas de A. oryzae (nas temperaturas de 10 e 55 °C) e de K. lactis (nas temperaturas de 10 e 37 °C) após 2 horas de reação. A eficiência de hidrólise foi avaliada em 2 horas de reação considerando a possível aplicação industrial das enzimas no referido processo.
Tabela 1. Eficiência da hidrólise da lactose do leite pelas β-galactosidases de A. oryzae e K. lactis nas concentrações de 3, 6 e 9 U/mL em 2 horas de reação.
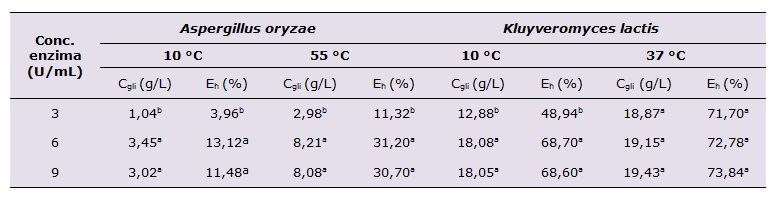
Observa-se que não há diferença significativa (p<0,05) entre as eficiências de hidrólise da lactose presente no leite, quando foram empregadas concentrações de 6 e 9 U/mL, para ambas as enzimas nas temperaturas ótimas e de 10ºC. Porém, para a concentração de 3 U/mL, a eficiência foi significativamente menor (p<0,05) na maioria das condições avaliadas.
Em 2 horas de reação, para uma mesma concentração de enzima, a β-galactosidase de K. lactis apresentou maior eficiência de hidrólise que a β-galactosidase de A. oryzae. Provavelmente esse resultado ocorreu devido ao pH da matéria-prima.
O pH do leite reconstituído utilizado nesse estudo apresentou valores de aproximadamente 6,8. A β-galactosidase de A. oryzae empregada apresenta pH ótimo na faixa de 4,5-5,0 e a de K. lactis entre 7,3-7,7.
As máximas eficiências de hidrólise da lactose, em 2 horas de reação, foram obtidas utilizando a β-galactosidase de K. lactis na temperatura de 37 ºC (Tabela 1). A maior taxa de conversão foi de 73,84% com 9 U/mL de enzima. Para a β-galactosidase de K. lactis, em nenhuma das condições avaliadas, atingiu-se 100% de eficiência de hidrólise (Figuras 1c e 1d).
Conclusão
Os resultados obtidos indicam que na temperatura de 10 ºC a enzima β-galactosidase de K. lactis é mais eficiente para a hidrólise da lactose presente no leite que a de A. oryzae. No entanto, nas condições de tempo de reação e concentração enzimática avaliadas, não foram atingidos 100% de hidrólise da lactose utilizando a β-galactosidase de K. lactis.
Referências
Freitas, F. F.; Marquez, L. D. S.; Ribeiro, G. P.; Brandão, G. C.; Cardoso, V. L.; Ribeiro, E. J. A comparison of the kinetic properties of free and immobilized Aspergillus oryzae β – Galactosidase. Biochemical Engineering Journal, v. 58-59, p. 33-38, 2011.
Gürdas S.; Guleç A.; Mutlu M. Immobilization of Aspergillus oryzae β galactosidase onto duolite A568 resin via simple adsorption mechanism. Food Bioprocess Technology, v. 5, p. 904-911, 2012.
Husain, Q. Β-Galactosidases and their potential applications: a review. Critical Reviews in Biotechnology, Boca Raton, v. 30, p. 41-62, 2010.
Mattar, R.; Mazo, D. F. C. Intolerância à lactose: mudança de paradigmas com a biologia molecular. Revista da Associação Médica Brasileira, São Paulo, v. 56, p. 230-236, 2010.
Pereira, P. C. Milk nutritional composition and its role in human health. Nutrition, London, v. 30, p. 619-627, 2014.
Leia também > Hidrólise enzimática da lactose em soros lácteos

 FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS
FAÇA SEU LOGIN E ACESSE CONTEÚDOS EXCLUSIVOS